题目内容
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02 mg/L。下列措施中能够减少SO2 排放量的是( )
①用天然气代替煤炭做民用燃料 ②提高热能利用率 ③硫酸厂采用更好的催化剂使SO2氧化成SO3 ④使用CS2萃取煤炭中的硫 ⑤燃煤中加入石灰后再使用
A.①②⑤ B.①③⑤
C.①③④ D.③④⑤
硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。已知:
①Na2S2O3·5H2O是无色晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
②向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3。
③Na2S2O3在20 ℃和70 ℃时的溶解度分别为60.0 g和212 g
Ⅰ 【制备产品】
实验装置如下图所示(省略夹持装置):
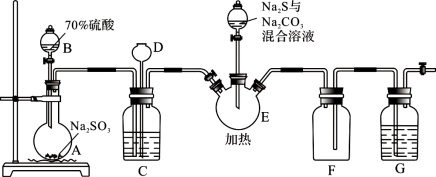
(1)仪器D的名称是 ;G中的试剂是 。
(2)装置C的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和NaHSO3溶液 c.饱和NaHCO3溶液
Ⅱ 【纯度检验】
取所得产品5.0 g,配成250 mL溶液。
(3)填写下表中的空白
实验方案 | 现象 | 结论 |
①取少量溶液于小试管中,滴加足量BaCl2溶液 | 有白色沉淀生成 | 产品中一定含有杂质 |
②将①所得混合液过滤,向洗涤后的沉淀滴加过量稀盐酸,加热,并用湿润的品红试纸置于管口 |
| 产品中含Na2SO4 |
品红试纸不褪色 |
|
产品中形成Na2SO4的可能原因是 。
(4)取25.00 mL溶液于锥形瓶中,滴加几滴淀粉作指示剂,用0.050 mol/L的标准碘水溶液滴定,重复三次,平均消耗标准碘水20.00 mL。滴定终点的现象是 ,产品中的Na2S2O3·5H2O的纯度为 。(已知:I2+2Na2S2O3=2NaI+Na2S4O6)
(5)粗Na2S2O3·5H2O可通过 方法提纯。


 H++OH-平衡,加入下列哪种物质或进行哪项操作,不会使平衡
H++OH-平衡,加入下列哪种物质或进行哪项操作,不会使平衡 体积一定小于11.2L。
体积一定小于11.2L。 况下,11.2L水中含有分子数为0.5NA
况下,11.2L水中含有分子数为0.5NA