��Ŀ����
 �籾��������仯�����2009��12��7�տ�Ļ�������ͱ����ԡ���ʷ��������Ҫ�Ļ��顱�����ı�������˵Ļ��顱�ȸ���������ͷ�Σ���Ȼ��������Ծͼ�����������ż��Ľ���������̼���������õ��˹㷺��ͬ���й��������¹��2010��11��5�Ŵ����ĵ�̼֮��--���������ٻص���ǰ���õ�̼�������뵽ÿ���˵�����֮�У���̼��ÿ���˵����Σ�����Դ�����е�ȼ�ϵ���ǵ�̼�о�����Ҫ����
�籾��������仯�����2009��12��7�տ�Ļ�������ͱ����ԡ���ʷ��������Ҫ�Ļ��顱�����ı�������˵Ļ��顱�ȸ���������ͷ�Σ���Ȼ��������Ծͼ�����������ż��Ľ���������̼���������õ��˹㷺��ͬ���й��������¹��2010��11��5�Ŵ����ĵ�̼֮��--���������ٻص���ǰ���õ�̼�������뵽ÿ���˵�����֮�У���̼��ÿ���˵����Σ�����Դ�����е�ȼ�ϵ���ǵ�̼�о�����Ҫ������1����ȼ�Ե��л���������������϶�������Ϊȼ�ϵ���еķ�Ӧ�����CxHyOz��ʾȼ�ϵ���е��л���Ӧ�O2Ϊ������Ӧ�40%��KOH��ҺΪ�������Һ����д��CxHyOz-O2-KOHȼ�ϵ�صĸ����ĵ缫��Ӧʽ��
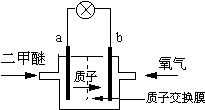
��2���ijǴ�ѧ������һ�����͵����ӽ���Ĥ������ȼ�ϵ�أ�DDFC�����õ���нϸߵİ�ȫ�ԣ�����ܷ�ӦΪ��CH3OCH3+3O2=2CO2+3H2O�����ʾ������ͼ������˵������ȷ���ǣ�
A��a��Ϊ��صĸ���
B����ع���ʱ������b���ص��߾������ٵ�a��
C����������ĵ缫��ӦΪ��O2+2H2O+4e-=4OH-
D����ع���ʱ��1mol�����ѱ�����ʱ��6mol����ת��
��3������C3H8-O2-KOH����ȼ�ϵ�أ�����11�˱����ڵ�صĸ�����ȫ��Ӧ�����ڵ�ص����·��ת�Ƶĵ��ӵ����ʵ���Ϊ
��4����һ��������C3H8-O2-KOHȼ�ϵ�ذ�һ����ʽ���д������߲�����ɵ��������������Ҫ�ĵ�ѹ�����øõ������500mLijCuSO4��ϡ��Һ���������Һ��Ҫ����98��Cu��OH��2����ʹ��Һ�ָ���ԭ����ͭ��Һ��Ũ�Ⱥ������������Ե�����ڵ������е�������ʧ��������ȫ���������CuSO4��Һ�����㣺
��ԭCuSO4����Һ��Ũ�ȣ�
�ڸõ�������ĵı����ڱ�״��ʱ�������
��������1��ȼ�ϵ���У�������ȼ�Ϸ���ʧ���ӵ�������Ӧ��
��2��A��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫�Ǹ�����
B����ع���ʱ�����������ص��ߵ�������
C��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫��������
D�����ݵ�ط�Ӧ��ȷ������ת�Ƶ���Ŀ��
��3�����ݱ���ȼ�յĻ�ѧ����ʽ���Ȼ�ѧ����ʽ�ĺ������ش�
��4�����ݷ�Ӧ2CuSO4+2H2O
2Cu��+O2��+2H2SO4���������ҺҪ��ԭԭ���ǣ���ʲô��ʲô����Ҫ����98��Cu��OH��2����ʹ��Һ�ָ���ԭ����ͭ��Һ��Ũ�Ⱥ�������˵��ԭ��Һ��1molCuSO4���ʵ��������ɵ�H2SO4��Һ�����˵�⣬����1molH2O�����˵�⣬����ȷ��ת�Ƶ��ӵ���Ŀ��ȷ��CuSO4����Һ��Ũ�ȣ����ݵ����غ���ȷ���õ�������ĵı���������
��2��A��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫�Ǹ�����
B����ع���ʱ�����������ص��ߵ�������
C��ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫��������
D�����ݵ�ط�Ӧ��ȷ������ת�Ƶ���Ŀ��
��3�����ݱ���ȼ�յĻ�ѧ����ʽ���Ȼ�ѧ����ʽ�ĺ������ش�
��4�����ݷ�Ӧ2CuSO4+2H2O
| ||
����⣺��1����ȼ�ϵ���У������������������õ��ӵķ�Ӧ��ԭ��Ӧ��O2+2H2O+4e-=4OH-��������ȼ��CxHyOz����ʧ���ӵ�������Ӧ���������ϸ�����Ӧ��Ϊ�ܵ�ȼ��ȼ�շ�Ӧ����ʽ��������Ӧ�����ܷ�Ӧ��ȥ������Ӧ����CxHyOz+��6x+y-2z��OH--��4x+y-2z��e-=xCO32-+��3x+y-z��H2O��
�ʴ�Ϊ��CxHyOz+��6x+y-2z��OH--��4x+y-2z��e-=xCO32-+��3x+y-z��H2O��
��2��A��ȼ�ϵ���У�ͨ��ȼ�϶����ѵĵ缫a�Ǹ�������A��ȷ��
B����ع���ʱ����������b�ص��ߵ�����a����B��ȷ��
C��ȼ�ϵ���У�ͨ�������ĵ缫�������������Ի����µĵ缫��ӦΪ��O2+4OH-+4e-=2H2O����C����
D�����ݵ�ط�ӦCH3OCH3+3O2=2CO2+3H2O��֪������ת�Ƶ���Ŀ��12����D����
��ѡCD��
��3�����ݱ���ȼ�յĻ�ѧ����ʽ��C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l����֪��������44g����ʱ��ת�Ƶ��ӵ����ʵ�����20mol�����Ե���11�˱����ڵ�صĸ�����ȫ��Ӧ�����ڵ�ص����·��ת�Ƶĵ��ӵ����ʵ���Ϊ5mol��1molCO2������KOH��Һ��Ӧ�ų�������ΪB KJ����3molCO2������KOH��Һ��Ӧ�ų�������Ϊ3B KJ������11�˱����ڵ�صĸ�����ȫ��Ӧ�Ĺ����зų���������ΪA KJ������C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l���ų��������ǣ�4A-3B��KJ����C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l������H=-��4A-3B��KJ/mol���ʴ�Ϊ��5��C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l������H=-��4A-3B��KJ/mol��
��4����CuSO4��Һ�������ķ���ʽΪ��2CuSO4+2H2O
2Cu��+O2��+2H2SO4���뿪��Ӧ��ϵ���൱����CuO������Ҫ����98�ˣ�1mol��Cu��OH��2����ʹ��Һ�ָ���ԭ����ͭ��Һ��Ũ�Ⱥ�������˵��ԭ��Һ��1molCuSO4���ʵ��������ɵ�H2SO4��Һ�����˵�⣬����1molH2O�����˵�⣬ת�Ƶĵ�������Ϊ4mol����ת��4mol����ʱ������Cu2++2e-=Cu��֪ͭ���ӵ����ʵ���Ϊ2mol������ԭCuSO4����Һ��Ũ��c=
=4mol/L����ԭCuSO4����Һ��Ũ��4mol/L��
�ڸ��ݱ���ȼ�յĻ�ѧ����ʽ��C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l����֪��������44g����ʱ��ת�Ƶ��ӵ����ʵ�����20mol����C3H8��20e-����ת��4mol����ʱ�����ı��������0.2mol�������0.2mol��22.4L/mol=44.8L���𣺸õ�������ĵı����ڱ�״��ʱ�����Ϊ44.8L��
�ʴ�Ϊ��CxHyOz+��6x+y-2z��OH--��4x+y-2z��e-=xCO32-+��3x+y-z��H2O��
��2��A��ȼ�ϵ���У�ͨ��ȼ�϶����ѵĵ缫a�Ǹ�������A��ȷ��
B����ع���ʱ����������b�ص��ߵ�����a����B��ȷ��
C��ȼ�ϵ���У�ͨ�������ĵ缫�������������Ի����µĵ缫��ӦΪ��O2+4OH-+4e-=2H2O����C����
D�����ݵ�ط�ӦCH3OCH3+3O2=2CO2+3H2O��֪������ת�Ƶ���Ŀ��12����D����
��ѡCD��
��3�����ݱ���ȼ�յĻ�ѧ����ʽ��C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l����֪��������44g����ʱ��ת�Ƶ��ӵ����ʵ�����20mol�����Ե���11�˱����ڵ�صĸ�����ȫ��Ӧ�����ڵ�ص����·��ת�Ƶĵ��ӵ����ʵ���Ϊ5mol��1molCO2������KOH��Һ��Ӧ�ų�������ΪB KJ����3molCO2������KOH��Һ��Ӧ�ų�������Ϊ3B KJ������11�˱����ڵ�صĸ�����ȫ��Ӧ�Ĺ����зų���������ΪA KJ������C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l���ų��������ǣ�4A-3B��KJ����C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l������H=-��4A-3B��KJ/mol���ʴ�Ϊ��5��C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l������H=-��4A-3B��KJ/mol��
��4����CuSO4��Һ�������ķ���ʽΪ��2CuSO4+2H2O
| ||
| 2mol |
| 0.5L |
�ڸ��ݱ���ȼ�յĻ�ѧ����ʽ��C3H8��g��+5O2��g��=3 CO2��g��+4H2O��l����֪��������44g����ʱ��ת�Ƶ��ӵ����ʵ�����20mol����C3H8��20e-����ת��4mol����ʱ�����ı��������0.2mol�������0.2mol��22.4L/mol=44.8L���𣺸õ�������ĵı����ڱ�״��ʱ�����Ϊ44.8L��
������������һ���ۺ�֪ʶ��Ŀ������Ƕȹ㣬Ҫ��ѧ�����з����ͽ��������������ѶȺܴ�

��ϰ��ϵ�д�
�����Ŀ

