题目内容
16.烧烤肉类时会产生强烈的刺激性致癌物质3,4-苯并芘,结构简式如图,其分子式为( )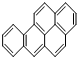
| A. | C20H12 | B. | C20H34 | C. | C22H12 | D. | C30H36 |
分析  由结构简式可知分子式,结构简式中含5个环状结构,C只能形成4个共价键,据此解答即可.
由结构简式可知分子式,结构简式中含5个环状结构,C只能形成4个共价键,据此解答即可.
解答 解:由结构简式可知分子中含20个C、12个H,则分子式为C20H12,故答案为:A.
点评 本题考查有机物的结构与分子式的书写判断,为高频考点,把握稠环结构及C形成4个共价键为解答的关键,侧重有机物结构分析及计算的考查,题目难度不大.

练习册系列答案
相关题目
10.化学与工农业生产、人类生活都有密切关系,下列说法中正确的是( )
| A. | 高纯度的二氧化硅晶体广泛用作制造光导纤维和太阳能电池板材料 | |
| B. | 铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝 | |
| C. | 高温下杀死H7N9,不属于蛋白质变性 | |
| D. | 用含有橙色酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的挥发性和还原性 |
6.U、V、W、Y、Z是原子序数依次增大的短周期主族元素,U、Y在周期表中的 相对位置如表:U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.
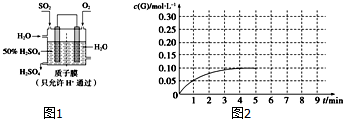
(1)元素Z在周期表中位于第VIIA族族,我国首创以W组成的金属一海水一空气电池作为能源的新型海水标志灯,它以海水为电解质溶液,靠空气中的氧气使W组成的金属不断氧化而产生电流.只要把灯放入海水中数分钟就会发出耀眼的白光.则该电源负极反应为Al-3e-=Al3+.
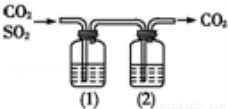
(2)YO2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VO,有关反应的离子方程式为3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+.由此可知YO2和VO还原性较强的是(写化学式)SO2.
(3)V的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境.其化学方程式为2NH3+3H2O2=N2+6H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下 表中反应条件x,该平衡体系中随x递增y递增的是bc(填代号).
③向含4mol/V的最高价含氧酸的稀溶液中.逐渐加入Fe粉,假设生成的气体只有一种(VO).
当加入的Fe粉质量为70g时.溶液中n(Fe3+):n(Fe2+)=2:3.
(4)相同温度下,等体积、物质的量浓度为0.1mol/L的KZ和CH3COOK溶液的两种
溶液中,离子总数相比较A(填代号)
A.前者多 B.-样多C.后者多 D.无法判断.
| U | ||
| Y |
(2)YO2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VO,有关反应的离子方程式为3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+.由此可知YO2和VO还原性较强的是(写化学式)SO2.
(3)V的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境.其化学方程式为2NH3+3H2O2=N2+6H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下 表中反应条件x,该平衡体系中随x递增y递增的是bc(填代号).
| 选 项 | a | b | C | d |
| X | 温度 | 温度 | 加入H2的 物质的量 | 加入甲的 物质的量 |
| V | 混合气体总质量与混合合气 体总物质的量之比 | 平衡常数 K | 混合气体的 密度 | 平衡时甲的 转化率 |
当加入的Fe粉质量为70g时.溶液中n(Fe3+):n(Fe2+)=2:3.
(4)相同温度下,等体积、物质的量浓度为0.1mol/L的KZ和CH3COOK溶液的两种
溶液中,离子总数相比较A(填代号)
A.前者多 B.-样多C.后者多 D.无法判断.
8.医疗上葡萄糖被大量用于病人输液的原因是( )
| A. | 葡萄糖是人体必需的营养素 | |
| B. | 葡萄糖由C.H、O三种元素组成 | |
| C. | 葡萄糖在人体内能直接进入新陈代谢 | |
| D. | 每克葡萄糖被氧化放出的能量值最大 |