题目内容
17.乙醇分子中不同的化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
| A. | 与金属钠作用时,键①断 | |
| B. | 燃烧时,①②③④⑤键均断裂 | |
| C. | 和乙酸、浓硫酸共热时,键②断裂 | |
| D. | 在银催化下和氧气反应时,键①和③断裂 |
分析 A.乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基中的O-H键;
B.燃烧是有机物最剧烈的反应了,所有的键都要断裂;
C.乙醇与酸发生酯化反应,酸脱羟基醇脱氢,断开的羟基中的O-H键;
D.乙醇在Ag催化下与O2反应生成乙醛和水,断开的是羟基中的O-H键和-OH所连的碳原子上C-H键.
解答 解:A.乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基中的O-H键,即键①断裂,故A正确;
B.燃烧是有机物最剧烈的反应,生成二氧化碳和水,所有的化学键都要断裂,故B正确;
C.乙醇与酸发生酯化反应,可以18O标记,研究反应机理:CH3COOH+CH3CH218OH$→_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O,故乙醇断键的位置为:①,故C错误;
D.乙醇在Ag催化下与O2反应生成乙醛和水,断开的是羟基中的O-H键和-OH所连的碳原子上C-H键,即断裂键①和③,故D正确,
故选C.
点评 本题主要考查了乙醇的化学性质,掌握反应的机理是解题的关键,难度不大,有机反应重在掌握反应中断键与成键位置.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
7.根据键能数据:H-Cl 431kJ/mol,H-I 299kJ/mol,由此可得出的结论是( )
| A. | 溶于水时,HI分子比HCl分子更容易电离 | |
| B. | HI比HCl熔、沸点都高 | |
| C. | HI比HCl更稳定 | |
| D. | 拆开相同物质的量的HI分子比HCl消耗的能量小,HI是离子化合物 |
5.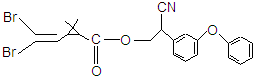 拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图.下列对该化合物叙述不正确的是( )
拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图.下列对该化合物叙述不正确的是( )
 拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图.下列对该化合物叙述不正确的是( )
拟除虫菊酯是一类高效,低毒,对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图.下列对该化合物叙述不正确的是( )| A. | 属于芳香化合物 | B. | 属于卤代烃 | ||
| C. | 具有酯类化合物的性质 | D. | 在一定条件下可以发生加成反应 |
12.向蔗糖晶体中加入一定量的浓硫酸,发现蔗糖晶体变黑、膨胀,此过程中浓硫酸没有表现的性质是( )
| A. | 脱水性 | B. | 强氧化性 | C. | 酸性 | D. | 吸水性 |
2.根据下列化学实验示意图及表中实验现象,从理论上分析得出的结论正确的是( )
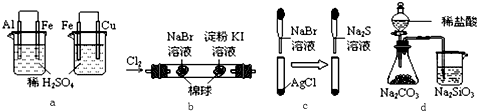

| 选项 | 实验 | 实验现象 | 结论 |
| A | a | 左烧杯中铁表面有气泡,右烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | b | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | c | 白色固体先变为淡黄色,后变为黑色 | 溶解度:AgCl<AgBr<Ag2S |
| D | d | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
9.已知热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ•mol-1(Q>0).下列说法中正确的是( )
| A. | 相同条件下,2 mol SO2(g)和1 mol O2(g)的键能之和大于2 mol SO3(g)的键能 | |
| B. | 一定量SO2(g)和O2(g)置于密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化 | |
| C. | 恒温恒压下,在上述已达到平衡的体系中加入高效催化剂,SO2的转化率一定增大 | |
| D. | 将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJ |
6. 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )| A. | 稀释前两溶液中H+浓度的大小关系:A=10B | |
| B. | 稀释前,A溶液中由水电离出的OH-的浓度大于10-7 mol/L | |
| C. | 取等体积M点的A、B两种碱液加入同浓度的硫酸溶液至恰好完全反应时,所消耗酸溶液的体积相同 | |
| D. | 用醋酸中和A溶液至恰好完全反应时,溶液的pH不一定大于7 |
16.下列说法中正确的是( )
| A. | 丙烯能使溴的四氯化碳溶液褪色,还可能在一定条件下与溴发生取代反应 | |
| B. | 正丁烷比丙烷难液化 | |
| C. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| D. | 乙醇的催化氧化也属于加成反应 |
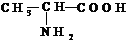 ,请回答下列问题.
,请回答下列问题.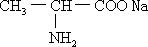 .
. 为:CH2=CHCN、CH2=CHCH=CH2、CH2=CHC6H5.
为:CH2=CHCN、CH2=CHCH=CH2、CH2=CHC6H5.