题目内容
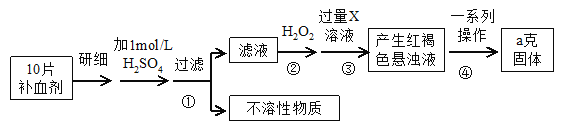
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外研究小组测定该补血剂中铁元素的含量,实验步骤如下:
请回答下列问题:
(1) 证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加 ,该过程的现象为: 。
(2) 步骤②加入过量H2O2的目的: 。
(3) 步骤③中反应的离子方程式: 。
(4) 步骤④中一系列处理的操作步骤:过滤、 、灼烧、 、称量。
(5) 若实验无损耗,则每片补血剂含铁元素的质量 g。
(6) 该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+=5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需 。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是 。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③滴定到终点时的颜色为 色。若滴定到终点时俯视滴定管刻度线,对测量值有何影响 ( 填 “偏高、偏低或无影响” )。
【答案】(1) 氯水(或双氧水等合理氧化剂);溶液由浅绿色变成血红色。
(2) 将Fe2+全部氧化成Fe3+ 。
(3) Fe3++3OH-=Fe(OH)3↓(或Fe3++3NH3·H2O= Fe(OH)3↓+ 3NH4+ )
(4) 洗涤 ;冷却
(5) 0.07a
(6) 250mL容量瓶; b ;紫(或紫红);偏低
【解析】
试题分析:(1)Fe3+遇KSCN溶液显红色,该现象用于检验Fe3+存在,可以加入氧化剂将Fe2+氧化为Fe3+.检验Fe2+可以先滴加KSCN溶液,溶液不变色,再滴加氯水或双氧水,溶液变为血红色,说明含有Fe2+,
(2)由流程图可知,该实验原理为:将药品中的Fe2+形成溶液,将Fe2+氧化为Fe3+,使Fe3+转化为氢氧化铁沉淀,再转化为氧化铁,通过测定氧化铁的质量,计算补血剂中铁元素的含量.步骤②加入过量H2O2的是将Fe2+氧化为Fe3+;
(3)步骤③是将Fe3+转化为氢氧化铁沉淀,试剂X可以是氢氧化钠或氨水等,反应离子方程式为Fe3++3OH-=Fe(OH)3↓(或Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+ );
(4)步骤④中一系列处理是由氢氧化铁悬浊液最终转化为氧化铁,需要过滤、洗涤的氢氧化铁,然后灼烧生成氧化铁,冷却后称量氧化铁的质量;
(5)最后氧化铁为ag,氧化铁含有铁元素的质量为![]() ×ag=0.7ag,故每片补血剂含铁元素的质量为
×ag=0.7ag,故每片补血剂含铁元素的质量为![]() =0.07ag;
=0.07ag;
(6)①精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管,250mL容量瓶;
②稀硝酸、浓硝酸具有强氧化性,含有氧化Fe2+,高锰酸钾可以氧化HCl为氯气,故选硫酸酸化;
③高锰酸钾为紫色,当滴定到终点时,Fe2+被完全氧化,加入的最后一滴高锰酸钾不反应,溶液的颜色为紫色.若滴定到终点时俯视滴定管刻度线,消耗高锰酸钾的体积偏小,测量值偏低。