题目内容
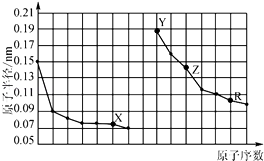
【题目】A、B、C、D、E、F的原子序数依次增大,它们都具有相同的核外电子层数。已知:A、C、F三种原子最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素的符号:A________,B________,E________。
(2)把B的单质(片状)放入滴有酚酞的沸水中,观察到的现象是_________________,反应的化学方程式是_______________________。
(3)A、C两种元素的最高价氧化物的水化物反应的离子方程式是____________。
【答案】 Na Mg P 产生气体,溶液变红 Mg+2H2O![]() Mg(OH)2+H2↑ Al(OH)3+OH-===AlO
Mg(OH)2+H2↑ Al(OH)3+OH-===AlO![]() +2H2O
+2H2O
【解析】试题分析:本题需要通过原子核外电子排布和相关化合物的性质推断六种元素,考查考生对原子核外电子排布的熟悉情况、考查基本实验现象、化学反应方程式、离子方程式等基础知识,考查考生对原子结构知识的综合运用能力及对试题的分析理解能力。
解析:(1)D元素原子的最外层电子数比次外层电子数少4,所以D次外层电子数为8,最外层电子数为4,D是Si元素,同理E为P元素。由此可知,这六种电子层数相同的元素均含有3个电子层,既都属于第三周期元素。“A、C、F三种元素的最高价氧化物的水化物之间两两皆能反应生成盐和水”,其中有一种必属于两性氢氧化物,为Al(OH)3,所以与Al(OH)3反应的碱只能是NaOH,既A为Na、C为Al,A、C最外层电子之和为4,则F最外层电子数为7,是Cl元素。A与C中间的元素只能是Mg。正确答案:Na、Mg、P。(2)Mg在沸水中发生反应Mg+2H2O![]() Mg(OH)2+H 2↑,反应过程中有气泡产生,且滴加酚酞的溶液变成红色。正确答案:产生气体且溶液变红、Mg+2H2O
Mg(OH)2+H 2↑,反应过程中有气泡产生,且滴加酚酞的溶液变成红色。正确答案:产生气体且溶液变红、Mg+2H2O![]() Mg(OH)2+H2↑ 。(3)A、C最高价氧化物的水化物分别是NaOH与Al(OH)3,二者反应的离子方程式Al(OH)3+OH-=AlO
Mg(OH)2+H2↑ 。(3)A、C最高价氧化物的水化物分别是NaOH与Al(OH)3,二者反应的离子方程式Al(OH)3+OH-=AlO![]() +2H2O。正确答案:Al(OH)3+OH-=AlO
+2H2O。正确答案:Al(OH)3+OH-=AlO![]() +2H2O。
+2H2O。

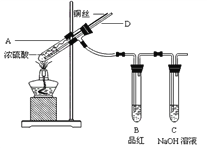
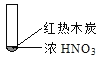
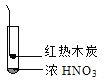
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸发生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应