题目内容
超细氮化铝粉末被广泛应用于大规模集成电路生产领域。其制取原理为:Al2O3+![]() 2AlN+3CO
2AlN+3CO
由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质,为测定该产品中有关成分的含量,进行了以下两个实验:
(1)称取

①上述反应的化学方程式为___________________________________。
②该样品中的AlN的质量分数为_______________。
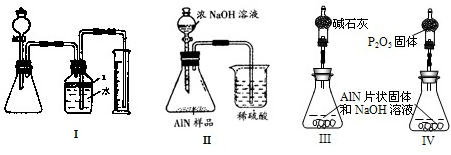
③在装置B中所选择的试剂是________________(填序号)。
a.H2O b.浓H2SO
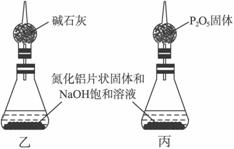
④上述实验方案,可能因气体体积测量不准,导致误差较大。有人建议改用下列乙、丙两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数。较合理的装置是___________(填代号)。
(2)另取
(1)①AlN+NaOH+H2O====NaAlO2+NH3↑
②61.5%
③c
④乙
(2)1.92
解析:(1)AlN+NaOH+H2O====NaAlO2+NH3↑
x
③选项所给物质中,只有CCl4因与NH3分子极性不同而不易溶解NH3,只有CCl4可用于NH3气体的测量。④碱石灰不吸收NH3且能防止水汽逸失,因而乙装置能通过测量反应前后装置的总质量算出AlN的质量,进而算出AlN的质量分数。P2O5既吸收NH3也吸收水汽,导致选用丙装置时不能测得足够的数据,不能计算出AlN的质量分数。(2)![]() =
=![]() 列
列![]() ,据CO2和CO含氧量列(2x+y)×
,据CO2和CO含氧量列(2x+y)×![]() ×
×