题目内容
微粒甲与离子乙在溶液中的转化关系如图所示: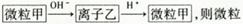 甲是
甲是
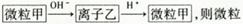 甲是
甲是| A.Si | B.NH4+ | C.Al | D.SO2 |
D
试题分析:A. Si+2OH-+H2O=SiO32-+2H2↑, SiO32-+2H+=H2SiO3↓.不能在产生原来的微粒。错误。B.NH4++OH-=NH3·H2O。NH3·H2O+H+= NH4++ H2O。但NH3·H2O不是离子。错误。C. 2Al+2OH-+2H2O=2AlO2-+3 H2↑, AlO2-+4H+=Al3++ 2H2O。错误。D.SO2+2OH- =SO32-+H2O;SO32-+2H+=SO2↑+H2O。正确。

练习册系列答案
相关题目

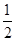 O2(g)=CO(g) ΔH=-110 kJ·mol-1
O2(g)=CO(g) ΔH=-110 kJ·mol-1 Fe(OH)3(胶体) +3H+
Fe(OH)3(胶体) +3H+ 2Cu+O2↑+4H+
2Cu+O2↑+4H+