题目内容
【题目】利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:

(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为 ;“水解”采用90℃而不在室温下进行的原因是 。
(2)“酸溶”时,Al2O3发生反应的离子方程式为 。
(3)“氧化”时,发生反应的离子方程式为________________________________。
(4)“废渣”成分为______________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是______________________。
(6)煅烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O] ![]() 2Al2O3 + 2NH3↑
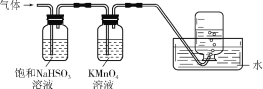
2Al2O3 + 2NH3↑ + N2↑ + 5SO3↑ + 3SO2↑ + 53H2O,将产生的气体通过如右图所示的装置。则集气瓶中收集到的气体是 (填化学式)。
+ N2↑ + 5SO3↑ + 3SO2↑ + 53H2O,将产生的气体通过如右图所示的装置。则集气瓶中收集到的气体是 (填化学式)。
【答案】(1)AlN+3H2O![]() Al(OH)3+NH3↑;降低NH3在水中的溶解度,促使NH3逸出;
Al(OH)3+NH3↑;降低NH3在水中的溶解度,促使NH3逸出;
(2)Al2O3+6H+═2Al3++3H2O;(3)2Fe2++2H++ClO-═2Fe3++Cl-+H2O;
(4)Fe(OH)3;(5)防止Al(OH)2Cl水解生成Al(OH)3(6)N2
【解析】
试题分析:分析工艺流程和信息知向铝灰(主要成分为Al、Al2O3、AlN、FeO等)中加水,90℃时,AlN水解生成氢氧化铝和氨气,然后加入盐酸酸溶,所得溶液为氯化铝、氯化亚铁和盐酸的混合液,加入漂白液,将Fe2+氧化为Fe3+,加入碳酸钠,Fe3+转化为氢氧化铁沉淀而除去,喷雾干燥得到产品。
(1)根据题意知气体A能使湿润的红色石蕊试纸变蓝,则A为氨气,则铝灰中AlN在90 ℃水解生成氢氧化铝和氨气,化学方程式为AlN+3H2O![]() Al(OH)3+NH3↑;“水解”采用90℃而不在室温下进行的原因是降低NH3在水中的溶解度,促使NH3逸出。
Al(OH)3+NH3↑;“水解”采用90℃而不在室温下进行的原因是降低NH3在水中的溶解度,促使NH3逸出。
(2)“酸溶”时,Al2O3与盐酸反应生成氯化铝和水,离子方程式为Al2O3+6H+═2Al3++3H2O。
(3)“氧化”时,溶液中的Fe2+在酸性条件下被漂白液中的ClO-氧化为Fe3+,发生反应的离子方程式为2Fe2++2H++ClO-═2Fe3++Cl-+H2O 。
(4)“废渣”成分为Fe(OH)3。
(5)采用喷雾干燥而不用蒸发的原因是防止Al(OH)2Cl水解生成Al(OH)3。
(6)缺少实验装置图,无法解析。