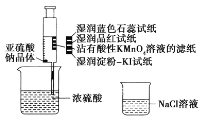
题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2LH2O中含有的质子数目为5NA
B.80mL10mol·L-1盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA
C.标况下11.2LNO和11.2LO2混合后所得气体分子数为NA
D.KClO3+6HCl=KCl+3Cl2↑+3H2O生成3molCl2转移5mol电子
【答案】D
【解析】
A. 标准状况下, H2O不是气体,11.2LH2O的物质的量不是0.5mol,故A错误;
B. 二氧化锰与稀盐酸不反应,80mL10mol·L-1盐酸与足量MnO2加热反应,参加反应的HCl的物质的量小于0.8mol,所以产生Cl2分子数小于0.2NA,故B错误;
C. ![]() ,
,![]() ,标况下11.2LNO和11.2LO2混合后所得气体分子数小于小于0.75NA,故C错误;
,标况下11.2LNO和11.2LO2混合后所得气体分子数小于小于0.75NA,故C错误;
D. KClO3+6HCl=KCl+3Cl2↑+3H2O,KClO3中氯元素化合价由+5降低为0、HCl中氯元素化合价由-1升高为0,氧化剂、还原剂的比为1:5,生成3molCl2转移5mol电子,故D正确;
选D。

练习册系列答案
相关题目
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g)ΔH<0,一段时间后达到平衡。反应过程中测定的数据如表
2Z(g)ΔH<0,一段时间后达到平衡。反应过程中测定的数据如表
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法不正确的是
A.反应前2min的平均速率v(Z)=2.0×10-3mol/(L·min)
B.其他条件不变,升高温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数不变