题目内容
A、B、C、D都是短周期元素,原子半径:D>C>A>B.已知:A、B同周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的3倍,下列说法正确的是( )
| A、A的元素符号为Be | B、B和D两种元素形成的化合物中只能含有离子键 | C、C和D两元素的最高价氧化物的水化物相互反应生成盐和水 | D、D2B和D2B2阴、阳离子个数比分别为1:2和1:1 |
分析:A、B、C、D都是短周期元素,原子半径:D>C>A>B.A、B同周期,A、C处于同一主族,可推知A、B、C、D在周期表中的大致相对位置为: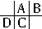 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,据此解答.
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,据此解答.
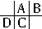 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,据此解答.
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,据此解答.解答:解:A、B、C、D都是短周期元素,原子半径:D>C>A>B.A、B同周期,A、C处于同一主族,可推知A、B、C、D在周期表中的大致相对位置为: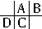 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,
A.由上述分析可知,A为B元素,故A错误;
B.O、Na形成的过氧化钠既含有离子键又含有共价键,故B错误;
C.C和D两元素的最高价氧化物的水化物分别为氢氧化铝、氢氧化钠,二者反应生成偏铝酸钠和水,故C正确;
D.Na2O(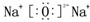 )和Na2O2
)和Na2O2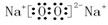 中阴、阳离子个数比都是1:2,故D错误,
中阴、阳离子个数比都是1:2,故D错误,
故选C.
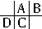 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,则D最外层电子数只能为1,故D为钠,C为Al,A为B元素,A.由上述分析可知,A为B元素,故A错误;
B.O、Na形成的过氧化钠既含有离子键又含有共价键,故B错误;
C.C和D两元素的最高价氧化物的水化物分别为氢氧化铝、氢氧化钠,二者反应生成偏铝酸钠和水,故C正确;
D.Na2O(
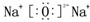 )和Na2O2
)和Na2O2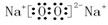 中阴、阳离子个数比都是1:2,故D错误,
中阴、阳离子个数比都是1:2,故D错误,故选C.
点评:本题考查元素位置结构性质的关系应用,题目难度中等,本题的关键是正确推断元素的种类,注意结合原子半径确定其在周期表中的相对位置.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目

