题目内容
25℃时,在一定体积pH=12的Ba(OH)2溶液中,逐滴滴加一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后的溶液体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
| A.1:9 | B.1:1 | C.1:2 | D.1:4 |
D
解析试题分析:设Ba(OH)2溶液的体积为V1,加一定物质的量浓度的NaHSO4溶液的体积为V2,因为Ba2+恰好完全沉淀,所以氢氧化钡与硫酸氢钠的物质的量是相等的。那么二者反应后,溶液中剩余的氢氧根离子为原来的一半,依题意有: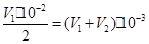
解之得:V1︰V2,=1︰4
考点:电解质的有关知识。

练习册系列答案
相关题目
关于NaHCO3溶液,下列表述不正确的是
| A.c (Na+)= c (HCO3-)+ c (CO32-)+ c (H2CO3) |
| B.c(Na+)+ c (H+)=" c" (HCO3-)+ c (CO32-)+ c (OH-) |
| C.HCO3-的水解程度大于HCO3-的电离程度 |
| D.c (H+) + c(H2CO3)=c (OH-)+ c(CO32-) |
W、X、Y、Z四种元素均为短周期元素且原子序数依次增大,其简单离子都能促进水的电离的是
| A.W2-、X+ | B.X+、Y3+ | C.X+、Z2- | D.Y3+、Z2- |
在醋酸的电离过程中,加入水会使下列比值增大的是
| A.c(CH3COOH)/c(CH3COO—) | B.c(CH3COO—)/c(OH—) |
| C.c(H+)/c(CH3COOH) | D.c(H+)/ c(OH—) |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A.pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH-)=c(H+) |
| B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| C.已知叠氮酸(HN3)与醋酸酸性相近,则在NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(OH¯)>c(N3¯)>c(H+) |
| D.0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L-1 HCN溶液与a mol·L-1 NaOH溶液等体积混合后,所得溶液显碱性(pH>7),则c (OH-)>c(H+)、c(Na+)>c(CN-)
C.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+) = c(OH-)+c(HCO3-)+c(CO32-)
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是(提示:BaSO4(s) Ba2+(aq)+SO42-(aq)的平衡常数Ksp = c(Ba2+)·c(SO42-),称为溶度积常数。)
Ba2+(aq)+SO42-(aq)的平衡常数Ksp = c(Ba2+)·c(SO42-),称为溶度积常数。)
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.d点无BaSO4沉淀生成 |
| C.通过蒸发可以使溶液由d点变到c点 |
| D.a点对应的Ksp大于c点对应的Ksp |
一定温度下的难溶电解质在水溶液中达到溶解平衡时。已知下表数据
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的PH值 | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是
A.向该溶液中加少量铁粉不能观察到红色固体析出
B.该溶液中c(SO42-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
C.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
D.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
某温度下,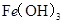
 分别在溶液中达到沉淀溶解平衡后,改变溶液
分别在溶液中达到沉淀溶解平衡后,改变溶液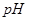 ,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
A. |
B.加适量 固体可使溶液由 固体可使溶液由 点变到 点变到 点 点 |
C.  两点代表的溶液中 两点代表的溶液中 与 与 乘积相等 乘积相等 |
D.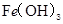 、 、 分别在 分别在 、 、 两点代表的溶液中达到饱和 两点代表的溶液中达到饱和 |