题目内容
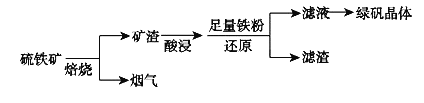
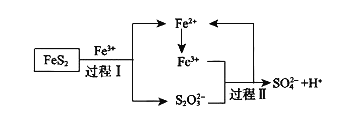
【题目】盐卤中除含有Mg2+、Cl﹣外,还含有少量Na+、Fe2+、Fe3+、SO42﹣和CO(NH2)2等.从海水提取食盐和Br2后的盐卤中可以提取MgCl2、MgO、Mg(OH)2等物质,制备流程如图所示:
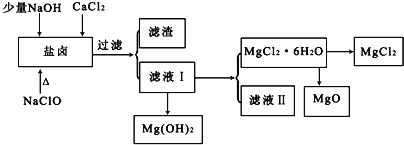
(1)从MgCl2溶液得到MgCl2.6H2O晶体的过程中所需的基本操作顺序依次为__________;
A 加热蒸馏 B 加热浓缩 C 冷却结晶 D 趁热过滤 E 过滤洗涤
(2)制取无水氯化镁必须在氯化氢存在的条件下进行,原因是___________(用适当的文字结合化学用语说明).
(3)用NaClO除去尿素CO(NH2)2时,生成物除盐外,都是能参与大气循环的物质,则该反应的化学方程式为___________;加入NaClO的另一个作用是___________.
(4)Mg(OH)2是制镁盐、耐火材料和阻燃剂的重要原料。
已知25℃时Ksp[Mg(OH)2]=5.6×10﹣12,且Mg(OH)2(s)═MgO(s)+H2O(s)△H=+81.5kJ/mol。
①下列叙述正确的是______
A.从盐卤或海水中获得Mg(OH)2,工业上选择NaOH作沉淀剂
B.Mg(OH)2能作阻燃剂的原因是它分解吸热且生成MgO覆盖可燃物
C.可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁
②酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,在Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为___________.
【答案】BCE 防止Mg2+水解,Mg2++2H2O Mg(OH)2+2H+ 3NaClO+CO(NH2)2═3NaCl+CO2↑+N2↑+2H2O
或NaOH+3NaClO+ CO(NH2)2═3NaCl+NaHCO3+N2↑+2H2O 氧化Fe2+使它变成Fe(OH)3沉淀而除去 B 蓝色
【解析】
向盐卤溶液中加入NaClO,NaClO具有强氧化性,能将Fe2+氧化为Fe3+,向盐卤中加入少量NaOH,NaOH和Fe3+反应生成Fe(OH)3,CO(NH2)2和NaClO发生氧化还原反应,生成物除盐外,都是能参与大气循环的物质,所以生成物是NaCl、CO2、N2、H2O,过量二氧化碳能和NaOH反应生成碳酸氢钠,将溶液过滤得到的滤渣是Fe(OH)3,滤液I中含有Mg2+、Cl﹣、Na+,将滤液I蒸发、结晶、过滤得到MgCl26H2O,则滤液中含有的杂质离子是Na+,直接将MgCl26H2O加强热能得到MgO,发生反应MgCl26H2O![]() MgO+2HCl↑+5H2O↑,氯化镁易水解,所以不能用加热MgCl26H2O方法制取氯化镁,要在HCl氛围中制取氯化镁。
MgO+2HCl↑+5H2O↑,氯化镁易水解,所以不能用加热MgCl26H2O方法制取氯化镁,要在HCl氛围中制取氯化镁。
(1)从MgCl2溶液得到MgCl2.6H2O晶体的过程,加热浓缩、冷却结晶、过滤洗涤,所以选择BCE。
(2)直接将MgCl26H2O加强热能得到MgO,同时还生成HCl和水蒸气,反应方程式为MgCl26H2O![]() MgO+2HCl↑+5H2O↑,氯化镁易水解,为防止氯化镁水解,在制取氯化镁时,要将MgCl26H2O放在氯化氢气体中,防止Mg2+水解,Mg2++2H2O Mg(OH)2+2H+。
MgO+2HCl↑+5H2O↑,氯化镁易水解,为防止氯化镁水解,在制取氯化镁时,要将MgCl26H2O放在氯化氢气体中,防止Mg2+水解,Mg2++2H2O Mg(OH)2+2H+。
(3)通过以上分析知,该反应为3NaClO+CO(NH2)2═3NaCl+CO2↑+N2↑+2H2O或NaOH+3NaClO+ CO(NH2)2═3NaCl+NaHCO3+N2↑+2H2O,次氯酸钠具有强氧化性,能将亚铁离子氧化为铁离子,再转化为氢氧化铁沉淀而除去。
(4)①A、从盐卤或海水中获得Mg(OH)2,工业上选择生石灰作沉淀剂,故A错误;B、Mg(OH)2分解吸热,且MgO不能燃烧,所以Mg(OH)2能作阻燃剂是它分解吸热且生成MgO覆盖可燃物,故B正确;C、MgO熔点太高,工业上电解氯化镁制取镁,故C错误;故答案为B;②25℃时,Mg(OH)2的溶度积Ksp=5.6×10﹣12,根据反应Mg(OH)2(s)Mg2++2OH﹣可得:c(Mg2+)c2(OH﹣)=5.6×10﹣12,
设c(OH﹣)=2c(Mg2+)=x,则:0.5x×x2=5.6×10﹣12,
解得:x=2.24×10﹣4mol/L,
c(H+)=![]() mol/L=4.5×10﹣11mol/L,
mol/L=4.5×10﹣11mol/L,
溶液的pH=10.4>9.6,所以溶液呈蓝色。

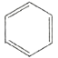
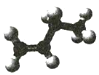
【题目】已知表中是某些有机物的模型图,根据要求回答下列问题:
有机物 | 甲 | 乙 | 丙 |
模型 |
|
|
|
(1)甲的分子式是___________________,其一氯代物有___________________种。
(2)写出乙与![]() 的
的![]() 溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
(3)丙的摩尔质量为![]() ,则用苯制备该物质时的催化剂是___________________。
,则用苯制备该物质时的催化剂是___________________。