题目内容
下列各组离子在指定溶液中一定能大量共存的是
| A.含有Fe3+的溶液中:Na+、AlO2一、C6H5-、I- |
| B.含有大量NO3-的溶液中:H+、Na+、Fe3+、Cl- |
| C.加入Al能放出H2的溶液中:Cl-、NO3-、SO42-、K+ |
| D.由水电离出的c(OH—)=l×10—13mol?L—1的溶液中:Na+、Ba2+、Cl-、NH4+ |
B
A项中Fe3+与AlO2-能发生双水解,与I-能发生氧化还原反应,不能大量共存,A项错误;B项中所有离子之间不反应,能大量共存,B项正确;加入Al能放出H2的溶液可以为酸性溶液,也可为碱性溶液,如果为酸性溶液,则NO3-不能大量共存,C项错误。由水电离出的c(OH-)=l×10—13mol?L—1的溶液可以为酸性溶液也可为碱性溶液,如为碱性溶液,则NH4+不能大量共存,D项错误。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
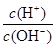 =1012的溶液:Fe2+、Mg2+、NO3-、Cl-
=1012的溶液:Fe2+、Mg2+、NO3-、Cl-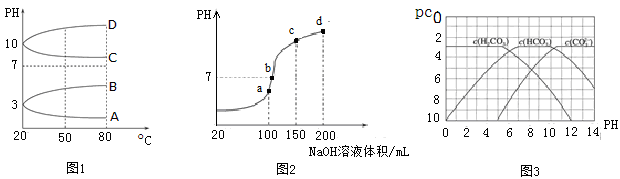
 H2CO3 H2CO3
H2CO3 H2CO3