题目内容
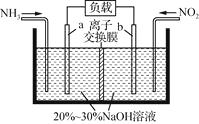
【题目】氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取。反应原理、实验装置图(加热装置都已略去)如下:
已知:氯苯为无色液体,沸点132.2℃,常温下不与氢氧化钠溶液反应。
回答下列问题:
(1)A反应器是利用实验室法制取氯气,中空玻璃管B的作用是。冷凝管中冷水应从(填“a”或“b”)处通入。
(2)把干燥的氯气通入装有干燥苯的反应器C中(内有相当于苯量1%的铁屑作催化剂),加热维持反应温度在40~60℃为宜,温度过高会生成二氯苯。
①对C加热的方法是(填序号)。
a.酒精灯加热 b.酒精喷灯加热 c.水浴加热
②D出口的气体成分有HCl、和。
(3)C反应器反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏。碱洗之前要水洗的目的是洗去部分无机物,同时减少碱的用量,节约成本。写出用10%氢氧化钠碱洗时可能发生的化学反应方程式:;(写两个即可)。
(4)上述装置图中A、C反应器之间,需要增添一个U形管,其内置物质是。
(5)工业生产中苯的流失情况如下:
项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
则1t苯可制得成品为t(只要求列式)。
【答案】
(1)平衡气压;a
(2)c;Cl2;苯蒸气
(3)HCl+NaOH=NaCl+H2O;FeCl3+3NaOH=Fe(OH)3↓+3NaCl;[Cl2+2NaOH=NaCl+NaClO+ H2O (任写两个)]
(4)五氧化二磷(或其他合理答案)
(5)![]()
【解析】解:(1)玻璃管B伸入液面下,装置内压强过大时,可以用于平衡气压;采取逆流原理通入冷凝水,使冷凝管充满冷凝水,充分冷却,即冷凝水由a口流入,由b口流出,
所以答案是:平衡气压;a;
(2)①反应器C加热控制反应温度在40-60℃,应利用水浴加热,故选:c;
②由于苯易挥发,反应产生的HCl,且有未反应的氯气,D出口气体中含有HCl、苯蒸汽、氯气,
所以答案是:苯蒸汽、氯气;
(3)②催化剂氯化铁与氢氧化钠反应,生成HCl会与氢氧化钠反应,溶解的氯气也会与去氧化钠反应,反应方程式为:FeCl3+3NaOH=Fe(OH)3↓+3NaCl、HCl+NaOH=NaCl+H2O、Cl2+2NaOH=NaCl+NaClO+H2O,
所以答案是:FeCl3+3NaOH=Fe(OH)3↓+3NaCl、HCl+NaOH=NaCl+H2O等;
(4)A、C反应器之间需要增添U型管,干燥生成的氯气,可以用五氧化二磷或氯化钙等,
所以答案是:五氧化二磷或氯化钙;
(5)苯的总流失量为89.2kg/t,故1t苯中参加反应的苯的质量为(1t-0.0892t),由苯与氯苯质量之比为78:112.5,可知生成氯苯质量为![]() t,
t,
所以答案是:![]() .
.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 |
H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
实验室用干燥、纯净的二氧化硫和氯气合成硫酰氯,装置如图所示(夹持仪器已省略),请回答有关问题:
(1)仪器A冷却水的进水口为(填“a”或“b”)。
(2)仪器B中盛放的药品是。
(3)实验时,装置丁中发生反应的离子方程式为。
(4)装置丙的作用为 , 若缺少装置乙,则硫酰氯会水解,该反应的化学
方程式为。
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+ SO2Cl2 , 此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的方法是。
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):。