题目内容
8.设NA为阿伏加德罗常数,下列叙述中正确的是( )| A. | 14 g乙烯和环丙烷的混合物中总原子数为3NA | |
| B. | 标准状况下,2.24L苯中约含有0.6NA个碳原子 | |
| C. | 4.6 g乙醇中含有的C-H键的个数为0.6NA | |
| D. | 1 mol  分子中含碳碳双键数为3NA 分子中含碳碳双键数为3NA |
分析 A、根据乙烯和环丙烷的最简式计算出含有的碳原子数;
B、标况下,苯为液态;
C、求出乙醇的物质的量,然后根据1mol乙醇中含5molC-H键来分析;
D、苯不是单双键交替的结构.
解答 解:A、乙烯和环丙烷的最简式为CH2,14g混合物中含有1mol最简式,含3mol原子,含有的原子数目为3NA,故A正确;
B、标况下,苯为液态,不能根据气体摩尔体积来计算其物质的量,故B错误;
C、4.6g乙醇的物质的量n=$\frac{4.6g}{46g/mol}$=0.1mol,而1mol乙醇中含5molC-H键,故0.1mol乙醇中含0.5molC-H键即0.5NA个,故C错误;
D、苯不是单双键交替的结构,结构中无碳碳双键,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
11.下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是( )
| 编号 | 化学反应 | 离子方程式 | 评价 |
| ① | 硫酸溶液中加入Ba(OH)2溶液 | Ba2++SO42-═BaSO4↓ | 正确 |
| ② | 氧化铝与NaOH溶液反应 | 2Al3-+302-+20H- ═2AlO2-+H20 | 错误,Al203不应写成离子 形式 |
| ③ | 铁和足量稀硝酸反应 | Fe+2H+═H2↑+Fe2+ | 正确 |
| ④ | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | 错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
| A. | ① | B. | ①③ | C. | ②④ | D. | ①②③④ |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA | |
| B. | pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 0.1 mol Na2O2晶体中含有0.3NA个离子 | |
| D. | 标准状况下,22.4L甲醇中含有的氧原子数为1.0NA |
16.构造原理揭示的电子排布能及顺序,实质是各能级能量高低顺序.则下列能级的能量高低顺序正确的是( )
| A. | 5s>4f>4s>3d | B. | 3d>4s>3p>3s | C. | 4s>3s>2s>1s | D. | 5s>4s>4f>3d |
3.下列说法中不正确的是( )
| A. | 用完的电池不可以随意地丢弃 | |
| B. | 增加炼铁高炉的高度可以降低尾气中CO的含量 | |
| C. | 加入催化剂可以大大提高化学反应速率 | |
| D. | 把煤粉碎后再燃烧可以提高煤的燃烧效率 |
13.向50mL 18mol•L-1H2SO4溶液中加入足量的铜片并加热.充分反应后,被还原的H2SO4的物质的量( )
| A. | 小于0.45 mol | B. | 等于0.45 mol | ||
| C. | 在0.45 mol和0.90 mol之间 | D. | 大于0.90 mol |
20.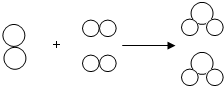 右图是用比例模型来表示某物质发生化学变化的微观示意图.图中
右图是用比例模型来表示某物质发生化学变化的微观示意图.图中 和
和 分别表示两种元素的原子,能用该图表示的化学反应是( )
分别表示两种元素的原子,能用该图表示的化学反应是( )
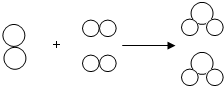 右图是用比例模型来表示某物质发生化学变化的微观示意图.图中
右图是用比例模型来表示某物质发生化学变化的微观示意图.图中 和
和 分别表示两种元素的原子,能用该图表示的化学反应是( )
分别表示两种元素的原子,能用该图表示的化学反应是( )| A. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | B. | 2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO | ||
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | D. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 |
17.一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)?Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
| A. | 混合气体的密度不再变化 | |
| B. | 反应容器中Y的质量分数不变 | |
| C. | X的分解速率与Y的消耗速率相等 | |
| D. | 单位时间内生成1 mol Y的同时生成2 mol X |