题目内容
2.重水(D2O)主要用于核反应堆中中子的减速剂和冷却剂,在化学和生物学中,重水常用作示踪物质来研究反应机理等.下列说法正确的是( )| A. | D是氢的一种核素,原子核内有2个中子 | |
| B. | 1H218O与D216O的相对分子质量相同 | |
| C. | 3H2O与D2O互称同位素 | |
| D. | 通过化学变化可以直接实现普通水向重水转化 |
分析 A.中子数=质量数-质子数;
B.相对分子质量=各原子的相对原子质量的和;
C.具有相同质子数、不同中子数的原子互为同位素;
D.同位素之间的转化属于核变化.
解答 解:A.中子数=质量数-质子数=2-1=1,故A错误;
B.1H218O与D216O的相对分子质量都为20,故B正确;
C.3H2O与D2O均为水,属于化合物,不是原子,故C错误;
D.普通水向重水转化没有新物质生成,属于核变化,故D错误.
故选B.
点评 本题考查同素异形体及同位素,把握相关的概念及核变化为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
13.不小心使皮肤粘上了高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)稀溶液洗涤,黑斑可迅速褪去,其离子方程式为:MnO4-+H2C2O4+H+→CO2↑+Mn2++ ,下列有关叙述正确的是( )
| A. | 发生还原反应的是:H2C2O4 | |
| B. | 该离子方程式右侧横线上的产物是OH- | |
| C. | 10 mol二氧化碳生成时,电子转移5 mol | |
| D. | 通常用H2SO4溶液而不用盐酸酸化KMnO4溶液 |
10.如表是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最活泼的非金属原子的原子结构示意图为 .
.
(2)地壳中含量最多的金属元素是Al(写元素符号).
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是K0H,呈两性的氢氧化物是Al(OH)3.
(4)写出⑤与氢氧化钠反应的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
写出⑤的氢氧化物与氢氧化钠溶液完全反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.(2)地壳中含量最多的金属元素是Al(写元素符号).
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是K0H,呈两性的氢氧化物是Al(OH)3.
(4)写出⑤与氢氧化钠反应的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
写出⑤的氢氧化物与氢氧化钠溶液完全反应的离子方程式:Al(OH)3+OH-═AlO2-+2H2O.
17.键线式可以简明扼要的表示碳氢化合物, 这种键线式物质是( )
这种键线式物质是( )
 这种键线式物质是( )
这种键线式物质是( )| A. | 丁烷 | B. | 异丁烷 | C. | 异戊烷 | D. | 新戊烷 |
7.进行下列实验,由实验现象得出的结论正确的是( )
| A. | 某气体能使湿润的淀粉KI试纸变蓝,该气体一定是Cl2 | |
| B. | 向某溶液中滴加KSCN溶液,溶液显红色,该溶液中含有Fe3+ | |
| C. | 向某溶液中逐滴滴加稀氨水至过量,先产生白色沉淀然后沉淀溶解,该溶液中含有Al3+ | |
| D. | 向某溶液中通入CO2溶液变浑浊,继续通CO2浑浊消失,该溶液可能是Na2SiO3溶液 |
12.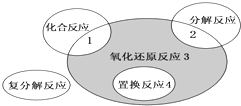 氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影3区域的是 ( )
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影3区域的是 ( )
 氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影3区域的是 ( )
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影3区域的是 ( )| A. | Cl2+2NaI═2NaCl+I2 | B. | CH4+2O2═CO2+2H2O | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2H2O2═2H2O+O2↑(MnO2催化下) |
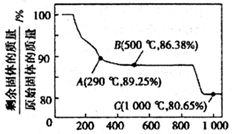 有报道称Co3O4能催化N2O分解,其中27Co在元素周期表中属于铁系元素,其单质及化合物的性质与铁有很多相似之处.
有报道称Co3O4能催化N2O分解,其中27Co在元素周期表中属于铁系元素,其单质及化合物的性质与铁有很多相似之处.