题目内容
【题目】某些简单有机物在一定条件下可发生如下转化,其中E(分子式C10H12O2)具有果香味:

请回答下列问题:
(1)F的分子式______________反应①的反应类型____________
(2)写出反应③的化学方程式________________________________________________
(3)下列说法中,正确的是_________
A. B分子中所有原子可能共平面 B.常温常压下物质B呈气态
C.1molB最多与4molH2发生加成 D.C与G是同系物
【答案】 C6H12O6 加成反应  AC
AC
【解析】A、 与乙炔加成得到B,B、
与乙炔加成得到B,B、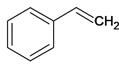 与水加成生成C、
与水加成生成C、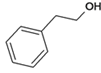 ,C经过连续氧化生成D,D、
,C经过连续氧化生成D,D、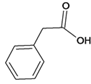 与g发生酯化反应生成E,E、
与g发生酯化反应生成E,E、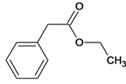 淀粉水解生成F、C6H12O6(葡萄糖),在酒化酶的作用下生成乙醇G
淀粉水解生成F、C6H12O6(葡萄糖),在酒化酶的作用下生成乙醇G![]() 。
。
(1)淀粉水解生成F的分子式C6H12O6(葡萄糖);A、 与乙炔加成得到B,反应①的反应类型加成反应;(2)D
与乙炔加成得到B,反应①的反应类型加成反应;(2)D 与g乙醇发生酯化反应生成E
与g乙醇发生酯化反应生成E ,反应③的化学方程式
,反应③的化学方程式 ;(3)A、 B
;(3)A、 B 分子中所有碳原子都是SP2杂化形成键角为1200的化学键,所有的原子可能共平面,故A正确;B、常温常压下物质B呈液态,故B错误;C、1molB最多与4molH2发生加成,苯环上要3mol,双键上1mol,故C正确; D、C属于芳香族化合物与G结构不相似,不是同系物,故D错误;故选AC。
分子中所有碳原子都是SP2杂化形成键角为1200的化学键,所有的原子可能共平面,故A正确;B、常温常压下物质B呈液态,故B错误;C、1molB最多与4molH2发生加成,苯环上要3mol,双键上1mol,故C正确; D、C属于芳香族化合物与G结构不相似,不是同系物,故D错误;故选AC。

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①哪一时间段时间段反应速率最大______min(填0~1、1~2、2~3、3~4、4~5),原因是____________。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率__________(设液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是__________。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)在一定温度下,将一定量的气体通入体积为2 L的密闭容器中,使其发生反应,有关物质X、Y、Z的物质的量的变化如图所示。

①则下列有关推断正确的是________________。
A.该反应的化学方程式是:3Z![]() 3X+2Y
3X+2Y
B.t0时,X、Y、Z的质量不再改变
C.t0时,Z的浓度为1.2 mol/L
D.t0时反应停止,反应速率为0
②t0时,Z的转化率为_____________。
③若t0=2min,则2min内用Y的浓度变化表示的反应速率为:________________。



