题目内容
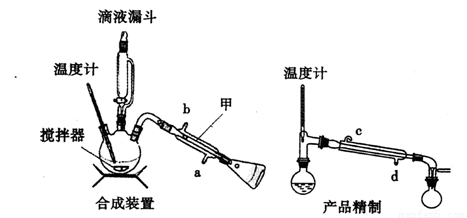
实验室可用碳酸钠合成亚硫酸钠晶体.有关装置如图所示:

将17g Na2CO3溶于80mL水中,分装在C、D两个锥形瓶中,再将25g铜屑放入圆底烧瓶中,将60mL浓硫酸和10mL水的混合液装在分液漏斗中,逐滴加入硫酸后,小心加热使SO2逐渐产生(注意控制气量大小和反应速率的快慢).将SO2通入Na2CO3溶液中至饱和,在合并C、D两瓶所得溶液中,慢慢加入17g Na2CO3,蒸发浓缩,冷却后得亚硫酸钠晶体.试回答:
(1)如何配制60mL浓硫酸与10mL水的混合液?答:________.
(2)装置B中浓硫酸的作用:________.
(3)Na2CO3溶液要分装在两个锥形瓶中的理由是:________;
写出C中发生反应的离子方程式
________.
(4)控制SO2产生速率的方法是________.
(5)通SO2结束后,加Na2CO3的目的是________.
答案:
解析:
解析:
|
(1)量取10mL蒸馏水放在烧杯中,沿玻璃棒将60mL浓硫酸慢慢倒入水中,同时不断搅拌. (2)干燥并除去酸雾,且可根据放出气泡的快慢判断SO2生长速率. (3)充分吸收SO2,2SO2+CO32-+H2O=CO2↑+2HSO3- (4)观察B瓶中出现气泡的快慢,用加热控制速率,当B中气泡放出太快,可移去酒精灯,待缓和后再用小火加热 (5)使NaHSO3转化为Na2SO3. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目