题目内容
临湘一中食堂以前烧煤,经过改造现在烧天然气,使校园环境有了很大的改善。天然气的主要成分是甲烷,若2克甲烷完全燃烧可放出QKJ的热量,请写出能表示甲烷燃烧热的热化学方程式 。
CH4(g) +2O2(g)=CO2(g) + 2H2O(l) △H="-8Q" kJ/mol
解析试题分析:2g甲烷的物质的量是2g÷16g/mol=0.125mol,若2克甲烷完全燃烧可放出QKJ的热量,则1mol甲烷完全燃烧生成CO2和液态水放出的热量为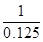 ×QKJ=8QkJ,所以反应的热化学方程式为CH4(g) +2O2(g)=CO2(g) + 2H2O(l) △H="-8Q" kJ/mol。
×QKJ=8QkJ,所以反应的热化学方程式为CH4(g) +2O2(g)=CO2(g) + 2H2O(l) △H="-8Q" kJ/mol。
考点:考查热化学方程式的书写

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
下列说法不正确的是(设NA为阿伏加德罗常数的数值)( )
| A.20g重水含有10NA个电子 |
| B.1L 0.1 mol·L-1 Na2SO3溶液中含有的SO32-数目少于0.1NA个 |
| C.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高 |
| D.用足量铜粉除去FeCl2溶液中的FeCl3杂质 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.46 g乙醇中含有的化学键数为7 NA |
| B.1 mol氯气和足量NaOH溶液反应转移电子数为2 NA |
| C.1 mol OH-和1 mol -OH(羟基)中含有的质子数均为 9 NA |
| D.10 L 0.1 mol·L-1的Na2CO3溶液中,Na+、CO32-总数为3 NA |
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为 mol·L-1。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)= mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是 (填序号)。
| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 |
| D.需要称量NaClO固体的质量为143.0 g |

(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为 mol·L-1。
②需用浓硫酸的体积为 mL。