题目内容
11. A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件和部分副产 物未标出),其中反应①是置换反应.
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件和部分副产 物未标出),其中反应①是置换反应.(1)若 A、D、F都是非金属单质,且A、D所含元素在周期表中同一列,A、F所含元素 在周期表中同一横行,则反应①的化学方程式是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(2)若 A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在 水溶液中进行)的离子方程式是2Fe2++Cl2=2Fe3++2Cl-;
(3)若B、C、F都是气态单质,且 B 有毒,③和④两个反应中都有水生成,反应②需要 放电才能发生,A、D相遇有白烟生成,反应③的化学方程式是4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O.
(4)若A、D为单质,且A原子核内所含质子数是D的2倍,B是参与大气循环的一种物质,③和④两个反应中都有红棕色气体生成,反应④的化学方程式是C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O.
分析 (1)短周期元素同主族元素之间的置换反应有多种,如Na→H2,O2→S,C→Si等,若A、D、F都是非金属单质,且A、D所含元素同主族,A、F所含元素 在周期表中同一横行,A、F所含元素同周期,则A为C,D为Si,F为O2;
(2)A是常见的金属单质,D、F是气态单质,由反应关系可知,A应为变价金属,则应为Fe,D、F是气态单质,应分别为H2、Cl2;
(3)若B、C、F都是气态单质,且B有毒,则B为Cl2,为Cl2和NH3的反应,生成N2和HCl;
(4)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,则A为Mg,D为C,为Mg和CO2的反应,③和④两个反应中都有红棕色气体生成,生成气体为NO2,则F为HNO3,以此解答该题.
解答 解:(1)短周期元素同主族元素之间的置换反应有多种,如Na→H2,O2→S,C→Si等,若A、D、F都是非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则A为C,D为Si,F为O2,反应①为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(2)A是常见的金属单质,D、F是气态单质,由反应关系可知,A应为变价金属,则应为Fe,D、F是气态单质,应分别为H2、Cl2,C生成E的反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)若B、C、F都是气态单质,且B有毒,则B为Cl2,为Cl2和NH3的反应,生成N2和HCl,NH3和氧气反应生成NO和水,为工业制硝酸的反应,化学方程式为
4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2 $\frac{\underline{催化剂}}{△}$4NO+6H2O;
(4)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,则A为Mg,D为C,为Mg和CO2的反应,③和④两个反应中都有红棕色气体生成,生成气体为NO2,则F为HNO3,反应④为C和硝酸的反应,方程式为C+4HNO3(浓 )$\frac{\underline{\;\;△\;\;}}{\;}$ 4NO2↑+CO2↑+2H2O,
故答案为:C+4HNO3(浓 )$\frac{\underline{\;\;△\;\;}}{\;}$ 4NO2↑+CO2↑+2H2O.
点评 本题考查元素化合物的推断,为高考常见题型,题目信息量大,难度较大,题目侧重于常见元素化合物的性质和用途来考查无机物的推断,学习中注重相关知识的积累.

 名校课堂系列答案
名校课堂系列答案| A. | 常温常压下,71g氯气与足量金属钠充分反应,转移的电子数为2 NA | |
| B. | 1.8g的NH4+离子中含有的电子数NA | |
| C. | 常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA | |
| D. | 1 mol/L MgSO4溶液中所含SO42-数目为NA |
| A | B | C | D | 单质E | |
| 熔点(℃) | 801 | 710 | 193 | -68 | 2300 |
| 沸点(℃) | 1456 | 1414 | 183 | 57 | 2500 |
| A. | D固体是共价化合物形成的晶体 | |
| B. | B中的键的强度比A中的键的强度大 | |
| C. | 单质E可能是原子之间由共价键直接形成的晶体 | |
| D. | C固体受热能升华 |
( )
| 物质 | ①NaF | ②NaI | ③MgO |
| 离子电荷数 | 1 | 1 | 2 |
| 离子的核间距 | 23.1nm | 31.8nm | 21.0nm |
| A. | ①>②>③ | B. | ③>②>① | C. | ③>①>② | D. | ②>①>③ |
| A. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2+O2 与 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O互为可逆反应 | |
| B. | 可逆反应在一定条件下可达到平衡状态,该状态下,正、逆反应速率相等,都为零 | |
| C. | 可逆反应不能进行到底,必然有反应物剩余 | |
| D. | 可逆反应的速率很小,达到最大限度时反应停止 |

| A. | 粗盐提纯,选①和② | B. | 用CCl4提取碘水中的碘,选③ | ||
| C. | 验证NH3易溶于水,选④ | D. | 除去Cl2中混有的HCl气体,选⑤ |
| A. | BeCl2 | B. | PCl3 | C. | PCl5 | D. | CH4 |
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | |
| B. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | 实验室用液溴和苯在催化剂作用下制溴苯: +Br2$\stackrel{FBr_{3}}{→}$ +Br2$\stackrel{FBr_{3}}{→}$ +HBr +HBr | |
| D. | 将CO2通入苯酚钠溶液:2 +CO2+H2O→2 +CO2+H2O→2 +Na2CO3 +Na2CO3 |
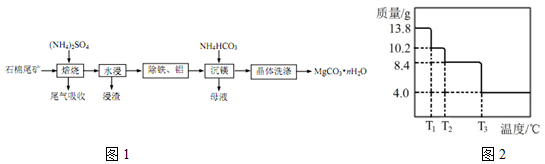
 .
.