题目内容
用NA表示阿伏加德罗常数的值。下列判断正确的是
| A.常温常压下,2 g H2含氢原子数为NA |
| B.标准状况下,32 g SO2的体积约为11.2 L |
| C.0.1 mol·L-1 NaNO3溶液中含有的钠离子数为NA |
| D.标准状况下,22.4 LH2O含有的氢原子数为2NA |
B
解析试题分析:A、2g氢气的物质的量是1mol,含氢原子数为2NA,A不正确;B、32gSO2的物质的量是32g÷64g/mol=0.5mol,在标准状况下的体积为0.5mol×22.4L/mol=11.2L,B正确;C、不能确定硝酸钠溶液的体积,无法计算钠的离子的个数,C不正确;D、标准状况下水不是气态,不能适用于气体摩尔体积,D不正确,答案选B。
考点:考查阿伏伽德罗常数的计算

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
元素周期表里金属元素和非金属元素分界线附近能找到
| A.制农药元素 | B.制催化剂元素 |
| C.制半导体元素 | D.制耐高温合金元素 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA |
B.标准状况下,2.24L氯气中含有的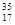 Cl数目一定为0.2NA Cl数目一定为0.2NA |
| C.常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA |
| D.80mL 10mol·L-1盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA |
下列有关化学用语不能表示2-丁烯的是( )
A.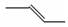 | B.CH3CH=CHCH3 | C.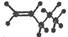 | D.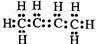 |
根据我国统一实行法定计量单位的规定,下列说法比较规范的是
| A.98g硫酸的摩尔数为1 mol |
| B.氧的摩尔质量为32g/mol |
| C.某硫酸中H2SO4的质量分数为0.60 |
| D.阿伏加德罗常数约为6.02×1023 个 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是(相对原子质量:D-2 O-16 Cu-64)
| A.18 g的D216O中含有的中子数为9 NA |
| B.物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA |
| C.33.6 L NO2溶于足量的水得到的溶液中含有的NO3-数为NA |
| D.32 g铜发生氧化还原反应,一定失去NA个电子 |
下列有关化学用语表示正确的是
| A.乙醛的结构简式:CH3COH |
B.H2O2的电子式: |
C.次氯酸的电子式: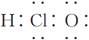 |
D.亚硫酸钠水解的离子方程式:SO32-+2H2O H2SO3+2OH- H2SO3+2OH- |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.在反应中消耗1mol Cl2,转移的电子数一定为2NA |
| B.标准状况下,0.5mol氦气含有的电子数为NA |
| C.15gCH3+(碳正离子)中含有电子数为10NA |
| D.0.1L 2 mol·L-1的(NH4)2S溶液中含有的S2-数目为0.2NA |
下列两种气体的分子数一定相等的是
| A.质量相等、密度不同的N2和C2H4 |
| B.体积相等的CO和N2 |
| C.等温、等体积的O2和N2 |
| D.等压、等体积的N2和CH4 |