题目内容
【题目】高锰酸钾是中学常用化学试剂,工业上常以软锰矿(主要成分是MnO2)为原料进行制备,主要工艺流程如下图:
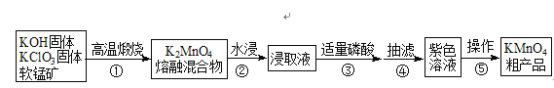
已知:3K2MnO4+2H3PO4═2KMnO4+MnO2↓+2K2HPO4+2H2O
物质 | KMnO4 | K2HPO4 | K2SO4 | CH3COOK | KCl | K2CO3 |
293K溶解度/g | 6.4 | 150 | 11.1 | 217 | 34 | 111 |
(1)原料高温煅烧时选用铁坩埚和铁棒,理由是__________。
(2)①中每生成1molK2MnO4时电子转移2mol,写出化学反应方程式_________。
(3)从反应机理和产物分离角度考虑,③可用磷酸,也可用下列________试剂。
A.醋酸 B.盐酸 C.硫酸 D.CO2
(4)下列描述不正确的是_________。
A.操作⑤中蒸发至大量晶体析出再冷却晶体,趁热过滤
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸
C.可用无水乙醇洗涤产品提高纯度
D.KMnO4晶体的烘干温度过高会降低产率
(5)粗产品的洗涤步骤可能需要用到以下操作:a.加入洗涤剂至浸没固体;b.洗涤剂缓慢通过;c.洗涤剂快速通过;d.关小水龙头;e.开大水龙头;f.重复2~3次。
请选出正确的操作并排序________。(操作可重复使用)
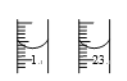
(6)高锰酸钾产品的纯度测定:准确称取0.7900g产品,配成250mL溶液,量取25.00mL于锥形瓶中,用0.1000molL﹣1(NH4)2Fe(SO4)2标准溶液进行滴定,滴定终点的现象__________。滴定前和滴定后的液面见下图。计算出高锰酸钾的纯度为_______。
【答案】高温下瓷坩埚和玻璃棒会与KOH等反应,与铁不反应 6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O AD ABC dabef 滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色 88.00%
3K2MnO4 +KCl+3H2O AD ABC dabef 滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色 88.00%
【解析】
(1)高温下瓷坩埚和玻璃棒中的二氧化硅和KOH等反应,被腐蚀,而铁坩埚和铁棒不反应。
(2)①中每生成1molK2MnO4时电子转移2mol,则生成3molK2MnO4时电子转移6mol;每1molKClO3参加反应转移电子6mol,根得失电子守恒,则KClO3与K2MnO4的物质的量比为1:3,则此反应的化学反应方程式为6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O。(3)根据表格中的数据CH3COOK和 K2CO3的溶解度比KMnO4大的多,蒸发浓缩基本上会留在母液中,其它的溶解度和KMnO4接近,会随KMnO4结晶析出。故BC不符合题意,AD符合题意。答案选AD。
3K2MnO4 +KCl+3H2O。(3)根据表格中的数据CH3COOK和 K2CO3的溶解度比KMnO4大的多,蒸发浓缩基本上会留在母液中,其它的溶解度和KMnO4接近,会随KMnO4结晶析出。故BC不符合题意,AD符合题意。答案选AD。
(4)A.操作⑤中蒸发至大量晶体析出,趁热过滤,防止出现大量的副产品,故A错误;
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸,故B正确。
C.不能用无水乙醇洗涤产品提高纯度,无水乙醇会与高锰酸钾反应,被高锰酸钾氧化,故C错误;
D.KMnO4受热易分解,KMnO4晶体的烘干温度过高会降低产率,应低温烘干,故D正确。(5)粗产品的洗涤步骤应为dabef的顺序排列。(6)高锰酸钾会与(NH4)2Fe(SO4)2发生氧化还原反应,当恰好反应时,高锰酸钾紫色刚好褪去,则滴定终点的现象为滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色;由图滴定前和滴定后的液面可知,滴定过程中消耗(NH4)2Fe(SO4)2溶液的体积为22.00mL。滴定过程中高锰酸钾和(NH4)2Fe(SO4)2发生氧化还原反应,高锰酸钾中锰元素价态由+7价降低到+2价生成Mn2+,(NH4)2Fe(SO4)2中Fe2+由+2价升高到+3价生成Fe3+,根据化合价升降守恒,高锰酸钾和(NH4)2Fe(SO4)2的物质的量比为1:5时恰好反应。过程中消耗n[(NH4)2Fe(SO4)2]=0.022L×0.1000molL﹣1=0.0022mol,则锥形瓶中25.00mL的高锰酸钾的物质的量为n(KMnO4)=0.0022mol÷5=0.00044mol,则250.00mL的高锰酸钾的物质的量0.0044mol,质量为m(KMnO4)=0.0044mol×158g/mol=0.6952g,则高锰酸钾的纯度为0.06952÷0.7900×100%=88.00%。
(1)高温下瓷坩埚和玻璃棒中的二氧化硅和KOH等反应,被腐蚀,而铁坩埚和铁棒不反应。本小题答案为:高温下瓷坩埚和玻璃棒会与KOH等反应,与铁不反应。
(2)①中每生成1molK2MnO4时电子转移2mol,则生成3molK2MnO4时电子转移6mol;每1molKClO3参加反应转移电子6mol,根得失电子守恒,则KClO3与K2MnO4的物质的量比为1:3,则此反应的化学反应方程式为6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O。本小题答案为:6KOH+KClO3+3MnO2
3K2MnO4 +KCl+3H2O。本小题答案为:6KOH+KClO3+3MnO2![]() 3K2MnO4 +KCl+3H2O。
3K2MnO4 +KCl+3H2O。
(3)根据表格中数据CH3COOK和 K2CO3的溶解度比KMnO4大的多,蒸发浓缩基本上会留在母液中,其它的溶解度和KMnO4接近,会随KMnO4结晶析出。故BC不符合题意,AD符合题意。答案选AD。
(4)A.操作⑤中蒸发至大量晶体析出,趁热过滤,防止出现大量的副产品,故A错误;
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸,故B正确。
C.不能用无水乙醇洗涤产品提高纯度,无水乙醇会与高锰酸钾反应,被高锰酸钾氧化,故C错误;
D.KMnO4受热易分解,KMnO4晶体的烘干温度过高会降低产率,应低温烘干,故D正确。答案选AC。
(5)粗产品的洗涤步骤应为dabef的顺序排列。本小题答案为:dabef。
(6)高锰酸钾会与(NH4)2Fe(SOspan>4)2发生氧化还原反应,当恰好反应时,高锰酸钾紫色刚好褪去,则滴定终点的现象为滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色;由图滴定前和滴定后的液面可知,滴定过程中消耗(NH4)2Fe(SO4)2溶液的体积为22.00mL。滴定过程中高锰酸钾和(NH4)2Fe(SO4)2发生氧化还原反应,高锰酸钾中锰元素价态由+7价降低到+2价生成Mn2+,(NH4)2Fe(SO4)2中Fe2+由+2价升高到+3价生成Fe3+,根据化合价升降守恒,高锰酸钾和(NH4)2Fe(SO4)2的物质的量比为1:5时恰好反应。过程中消耗n[(NH4)2Fe(SO4)2]=0.022L×0.1000molL﹣1=0.0022mol,则锥形瓶中25.00mL的高锰酸钾的物质的量为n(KMnO4)=0.0022mol÷5=0.00044mol,则250.00mL的高锰酸钾的物质的量0.0044mol,质量为m(KMnO4)=0.0044mol×158g/mol=0.6952g,则高锰酸钾的纯度为0.06952÷0.7900×100%=88.00%。本小题答案为:滴入最后一滴标准液,溶液紫红色恰好褪去,且半分钟内不变色;88.00%。

【题目】Ⅰ.下表是某位生物教师的肝肾糖脂血液化验单部分内容:
已知:1摩尔(mol)等于1000毫摩尔(mmol),血液中葡萄糖简称血糖,分子式为C6H12O6,请根据以上信息回答下列问题:
项目名称 | 数据 | 参考值 |
尿素氮 | 2.95 | 2.00﹣6.10mmol.L﹣1 |
葡萄糖 | 4.50 | 3.89﹣6.11mmol.L﹣1 |
总胆固醇 | 3.75 | <5.20mmol.L﹣1 |
甘油三酯 | 1.80↑ | <1.70mmol.L﹣1 |
(1)这位教师的血糖含量属___(填“正常”、“偏高”或“偏低”)。
(2)这位教师的1mL血液中含葡萄糖___g。
Ⅱ.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。表是500mL“鲜花保鲜剂”中含有的成分,阅读并回答下列问题:
成分 | 成分的质量(g) | 摩尔质量(gmol﹣1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.02 | 170 |
(1)下列“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为___。
(2)配制上述“鲜花保鲜剂”所的仪器有烧杯、玻璃棒、药匙、托盘天平(带砝码)、___(填所缺仪器的名称)。
(3)若要配制0.5mol/L500mL的硫酸溶液,现有质量分数为98%、密度为1.84g·cm﹣3的浓硫酸。实验室有15mL、20mL、50mL量筒,应选用___mL量筒最好。
【题目】高锰酸钾是中学常用化学试剂,工业上常以软锰矿(主要成分是MnO2)为原料进行制备,主要工艺流程如下图:
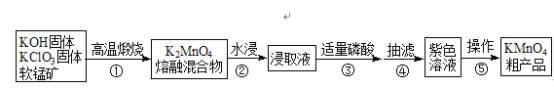
已知:3K2MnO4+2H3PO4═2KMnO4+MnO2↓+2K2HPO4+2H2O
物质 | KMnO4 | K2HPO4 | K2SO4 | CH3COOK | KCl | K2CO3 |
293K溶解度/g | 6.4 | 150 | 11.1 | 217 | 34 | 111 |
(1)原料高温煅烧时选用铁坩埚和铁棒,理由是__________。
(2)①中每生成1molK2MnO4时电子转移2mol,写出化学反应方程式_________。
(3)从反应机理和产物分离角度考虑,③可用磷酸,也可用下列________试剂。
A.醋酸 B.盐酸 C.硫酸 D.CO2
(4)下列描述不正确的是_________。
A.操作⑤中蒸发至大量晶体析出再冷却晶体,趁热过滤
B.抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸
C.可用无水乙醇洗涤产品提高纯度
D.KMnO4晶体的烘干温度过高会降低产率
(5)粗产品的洗涤步骤可能需要用到以下操作:a.加入洗涤剂至浸没固体;b.洗涤剂缓慢通过;c.洗涤剂快速通过;d.关小水龙头;e.开大水龙头;f.重复2~3次。
请选出正确的操作并排序________。(操作可重复使用)
(6)高锰酸钾产品的纯度测定:准确称取0.7900g产品,配成250mL溶液,量取25.00mL于锥形瓶中,用0.1000molL﹣1(NH4)2Fe(SO4)2标准溶液进行滴定,滴定终点的现象__________。滴定前和滴定后的液面见下图。计算出高锰酸钾的纯度为_______。