题目内容
10.下列表示物质结构的化学用语或模型图正确的是( )| A. | 乙烯的结构简式为CH2=CH2 | B. | CH4分子的比例模型: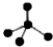 | ||
| C. | 8个中子的碳原子的符号:12C | D. | 氯化镁的电子式: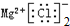 |
分析 A.乙烯分子中含有碳碳双键,结构简式中需要标出官能团结构;
B. 为甲烷的球棍模型,不是比例模型;
为甲烷的球棍模型,不是比例模型;
C.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.电子式书写不规范,氯离子不能合并,应该写在镁离子两边.
解答 解:A.乙烯分子中含有碳碳双键,乙烯的结构简式为:CH2=CH2,故A正确;
B.甲烷分子中含有4个碳氢键,比例模型主要体现出各原子的相对体积大小,甲烷正确的比例模型为: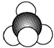 ,故B错误;
,故B错误;
C.碳原子的质子数为6,中子数为8的碳原子的质量数为14,该原子可以表示为:614C,故C错误;
D.氯化镁是离子化合物,由氯离子和镁离子构成,氯化镁正确电子式为: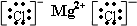 ,故D错误;
,故D错误;
故选A.
点评 本题考查常用化学用语的书写,题目难度中等,注意掌握常用化学用语的书写原则,注意离子化合物、共价键形成的物质的电子式书写方法及区别,试题培养了学生规范答题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要.天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳五个CH4分子或1个游离H2O分子若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为( )
| A. | CH4•14H2O | B. | CH4•8H2O | C. | CH4•($\frac{23}{3}$)H2O | D. | CH4•6H2O |
1.欲除去下列物质中混入的少量杂质(括号内为杂质),所选试剂和分离方法都正确的是( )
| A. | 甲烷(乙烯):KMnO4溶液 洗气 | B. | 苯(Br2):NaOH溶液 蒸馏 | ||
| C. | NaCl溶液(MgCl2):KOH溶液 过滤 | D. | 硝基苯(硝酸):蒸馏水 分液 |
5.下列有关有机物分离提纯或除杂的方法错误的是( )
| A. | 溴苯中混有溴,加NaOH溶液洗涤、静置、分液 | |
| B. | 除去乙醇中少量乙酸:加入足量生石灰蒸馏 | |
| C. | 乙酸乙酯中有乙酸杂质,可以加入饱和Na2CO3溶液,充分反应后静置分液 | |
| D. | 乙烯中混有SO2,将其通过盛有酸性KMnO4溶液的洗气瓶,再干燥 |
2.短周期主族元素X、Y、Z、W、R的原子序数依次增大.X与W同主族,X、W、R原子的最外层电子数之和为14,Y原子的最外层电子数是其内层电子数的3倍,W的单质是一种重要的半导体材料,Z是同周期主族元素中原子半径最大的元素.下列说法正确的是( )
| A. | Z、W是金属元素 | |
| B. | 原子半径:r(R)<r(W)<r(Z) | |
| C. | Y与Z形成的化合物只有一种 | |
| D. | X、Z、R的最高价氧化物对应的水化物之间都能相互发生反应 |
19.关于化学键的下列叙述中,正确的是( )
| A. | 凡金属元素与非金属元素化合时都能形成离子键 | |
| B. | 非金属原子间不可能形成离子键 | |
| C. | 钠原子与氯原子通过得失电子,以离子键结合成氯化钠后体系能量降低 | |
| D. | 含有共价键的化合物一定是共价化合物 |
17.可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极.下列说法不正确的是( )
| A. | 以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-=4OH- | |
| B. | 以NaOH溶液为电解液时,负极反应为Al+4OH--3e-=AlO2-+2H2O | |
| C. | 以NaOH溶液为电解液时,电池在工作过程中电解液的pH增大 | |
| D. | 以NaCl溶液为电解液时,电流由空气电极沿导线流向铝合金电极 |

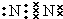 ,雷电作用能进行氮的固定,写出反应方程式N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO.
,雷电作用能进行氮的固定,写出反应方程式N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO.