题目内容
写出下列制取氯气的化学反应方程式:(1)实验室用二氧化锰跟浓盐酸反应制取氯气的化学反应方程式为_____________________。
(2)高锰酸钾(KMnO4)是常用的氧化剂,在酸性条件下,![]() 被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。
被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。
(3)历史上曾用“地康法”制取氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中氧气跟氯化氢反应制取氯气,化学反应方程式为__________________________。
从氯元素化合价的变化来看,以上三种方法的共同点是____________,比较以上三个反应,可得出三种氧化剂的氧化能力由强到弱的顺序为____________。
(1)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)2KMnO4+16HCl(浓)====2MnCl2+2KCl+5Cl2↑+8H2O
![]()
三个化学反应方程式中都是HCl中的Cl-被氧化剂氧化成Cl2 KMnO4>MnO2>O2
解析:第(1)小题源于教材,只要熟悉即能写出;第(2)(3)小题只要能很好地接受有关信息,具有良好的化学反应方程式的书写技能,就可迎刃而解。最后两问以本题的化学知识为依托,创设了自主学习、总结、探索的时间和空间。不难从三种获得氯气的化学反应原理中,根据氯元素在反应前后化合价的变化,得出上述三种方法的共同之处。从三个反应的反应条件,得出高锰酸钾、二氧化锰和氧气的氧化能力的相对强弱。

练习册系列答案
相关题目
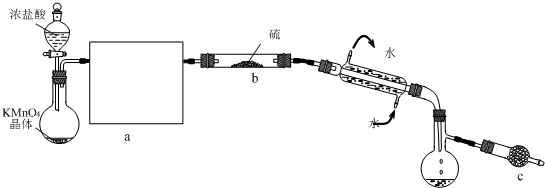

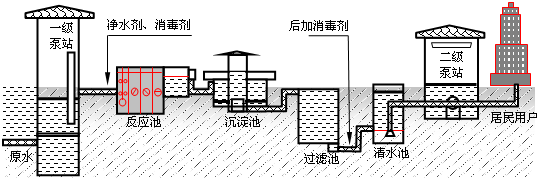
 HClO+H++Cl-
HClO+H++Cl-