题目内容
14.将下列物质分别加入到溴水中,溴水中溴单质的物质的量减少的是( )| A. | KCl | B. | KBr | C. | CCl4 | D. | I2 |
分析 分别加入溴水中,溴水中溴单质的物质的量明显减少,证明该物质可以和溴单质之间反应或者是产生萃取,或溴单质溶解于其他溶剂中.
解答 解:A.氯化钾和溴单质之间不会发生反应,溴水中溴单质的物质的量不会改变,故A错误;
B.溴单质和溴化钾之间不会发生任何反应,溴水中溴单质的物质的量不会改变,故B错误;
C.CCl4加入溴水中,溴水中溴单质在四氯化碳中的溶解度远远大于在水中的溶解度,所以溴单质会从水中转移向四氯化碳中,溴单质的物质的量明显减少,故C正确;
D.溴和碘不反应,溴的物质的量不变,故D错误.
故选C.
点评 本题考查物质的分离、提纯以及溴的性质,为高频考点,注意溴单质在四氯化碳中的溶解度远大于在水中的溶解度,理解萃取的原理是关键,难度中等.

练习册系列答案
相关题目
4.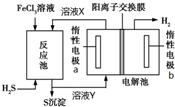 利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示.下列有关的说法错误的是( )
利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示.下列有关的说法错误的是( )
 利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示.下列有关的说法错误的是( )
利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示.下列有关的说法错误的是( )| A. | 惰性电极a为发生氧化反应 | |
| B. | Fe(OH)3胶体中滴加溶液X,先有沉淀后沉淀溶解 | |
| C. | 溶液Y加热蒸发灼烧最终得到Fe2O3 | |
| D. | 电解池总反应的离子方程式为2Fe2++2H+$\frac{\underline{\;电解\;}}{\;}$2Fe3++H2↑ |
5.将铝粉和某铁的氧化物粉末混合均匀后再均分为两等分.一份直接放入足量的烧碱溶液中充分反应;另一份在高温下恰好完全反应后再与足量的稀H2SO4反应.上述两种情况下生成的气体的质量比为4:3,则该铁的氧化物为( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | 无法确定 |
2.海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
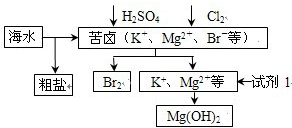

| A. | 试剂1可以选用石灰乳 | |
| B. | 从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2=2 Cl-+Br2 | |
| C. | 工业上,电解熔融MgO冶炼金属镁可减小能耗 | |
| D. | 粗盐经提纯后可用于制备氯气、钠等产品 |
9.下列有关离子检验的操作和实验结论都正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入氯化钡溶液,有白色沉淀生成,再加盐酸酸化,沉淀不溶解 | 该溶液中一定含有SO42- |
| B | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧 | CO2、H2O与Na2O2反应是放热反应 |
| C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该溶液中一定含有CO32- |
| D | 用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色 | 原溶液中不含K+ |
| A. | A | B. | B | C. | C | D. | D |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | pH=1的H2SO4溶液,含H+的数目为2NA | |
| B. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 | |
| C. | 273K,101kPa下,14g乙烯与丙烯混合物中含有碳原子数目为3NA | |
| D. | 0.2mol C2H6O分子中一定存在0.2NA个碳碳单键 |
3.下列说法不正确的是( )
| A. | 12C与14C为不同核素 | |
| B. | 石墨和C60的互为同素异形体 | |
| C. | H2O和D2O互为同位素 | |
| D. | 氨基酸分子中均含有羧基(-COOH)和氨基(-NH2) |
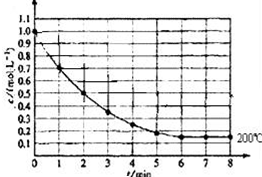 一固定体积的密闭容器中放入1molX(g)发生反应:X(g)?4Y(s)+Z(g),如图表示在 200℃时,X的浓度随时间变化的曲线.
一固定体积的密闭容器中放入1molX(g)发生反应:X(g)?4Y(s)+Z(g),如图表示在 200℃时,X的浓度随时间变化的曲线.