题目内容
【题目】2016年,美国研究小组开发出一种以糖为能源,可循环使用的环保电池装置。其工作原理如图所示。下列说法错误的是
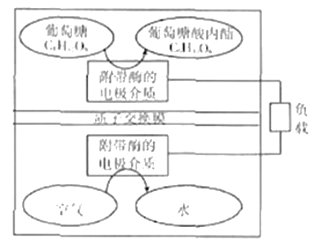
A. 葡萄糖在电池负极发生反应
B. 装置所示原理可以在强碱性条件下进行
C. 装置正极电极反应式为:O2+4e-+4H+=2H2O
D. 装置工作时,每消耗180g葡萄糖,将有2mol质子通过交换膜
【答案】B
【解析】A、该电池的总反应可以描述为:葡萄糖+O2→葡萄糖酸内酯+H2O,因此反应过程中葡萄糖被氧化,在原电池的负极参加反应,A正确。B、葡萄糖转变成葡萄糖酸内酯的过程需要“附带酶的电极介质”,而酶在强碱条件下会发生变性而失去活性,所以不宜在强酸、强碱等条件下进行,B错误。C、电池正负极间以质子交换膜分隔开,所以两极反应与质子(H+)有关,因此正极O2反应生成H2O的反应原理为:O2+4e-+4H+=2H2O,C正确。D、葡萄糖酸内酯结构是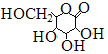 ,负极反应为:C6H12O6-2e-=C6H10O6+2H+,180g葡萄糖为
,负极反应为:C6H12O6-2e-=C6H10O6+2H+,180g葡萄糖为![]() ,则反应转移电子2 mol,D正确。所以错误答案选B。
,则反应转移电子2 mol,D正确。所以错误答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】已知几种难溶电解质的溶度积如下表所示:
几种难溶电解质的Ksp(25℃) | |
沉淀溶解平衡 | Ksp |
AgBr(s) | 5,0×10-13 mol2·L-2 |
AgI(s) | 8.3×10-17 mol2·L-2 |
FeS(s) | 6.3×10-18 mol2·L-2 |
ZnS(s) | 1.6×10-24 mol2·L-2 |
CuS(s) | 1.3×10-36 mol2·L-2 |
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺为:____________________。
(2)向饱和的AgI溶液中加入固体硝酸银,则c( I- )________(填“增大”、“减小”或“不变”),若改加AgBr固体,则c(Ag+)__________(填“增大”、“减小”或“不变”)。
(3)在25℃时,向100mL浓度均为0.1 mol·L-1 FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是_____________________(用沉淀物的化学式表示)。
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡: ZnS(s)![]() Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是 _______。
A.加入少量CuS固体 B.加入少量FeS固体
C.加入少量FeCl2固体 D.加入少量CuCl2固体


