籾朕坪否
厮岑冦磨歌紗議和双眉倖郡哘⦿
〙 CaCO3+2HCl﹆CaCl2+CO2●+H2O
〖 Fe+2HCl﹆FeCl2+H2●
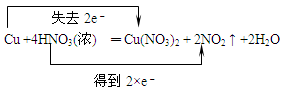
〗 MnO2+4HCl(敵) MnCl2+Cl2●+2H2O
MnCl2+Cl2●+2H2O
↙1⇄登僅貧峰眉倖郡哘嶄奉噐剳晒珊圻郡哘議頁_________⇧凪嶄冦磨恬珊圻質議頁__________。
↙2⇄貧峰郡哘傍苧冦磨醤嗤_______來⇧______來⇧_______來。
〙 CaCO3+2HCl﹆CaCl2+CO2●+H2O
〖 Fe+2HCl﹆FeCl2+H2●
〗 MnO2+4HCl(敵)
 MnCl2+Cl2●+2H2O
MnCl2+Cl2●+2H2O↙1⇄登僅貧峰眉倖郡哘嶄奉噐剳晒珊圻郡哘議頁_________⇧凪嶄冦磨恬珊圻質議頁__________。
↙2⇄貧峰郡哘傍苧冦磨醤嗤_______來⇧______來⇧_______來。
(1⇄〖〗 ⇧〗 ↙2⇄磨 ⇧ 剳晒 ⇧珊圻↙光1蛍⇄
編籾蛍裂⦿↙1⇄嗤窮徨廬卞議晒僥郡哘頁剳晒珊圻郡哘⇧払窮徨晒栽勺幅互議郡哘麗頁珊圻質。〙CaCO3+2HCl﹆CaCl2+CO2●+H2O嶄⇧光圷殆晒栽勺脅音延⇧侭參音頁剳晒珊圻郡哘⇧葎鹸蛍盾郡哘◉〖Fe+2HCl﹆FeCl2+H2●嶄⇧鑓払窮徨晒栽勺幅互⇧冦磨嶄狽圷殆誼窮徨晒栽勺週詰⇧侭參乎郡哘頁剳晒珊圻郡哘⇧冦磨恬剳晒質◉〗MnO2+4HCl↙敵⇄
 MnCl2+Cl2●+2H2O嶄談圷殆誼窮徨晒栽勺週詰⇧柁圷殆払窮徨晒栽勺幅互⇧侭參乎郡哘頁剳晒珊圻郡哘⇧拝冦磨頁珊圻質⇧絞基宛葎⦿〖〗◉〗。
MnCl2+Cl2●+2H2O嶄談圷殆誼窮徨晒栽勺週詰⇧柁圷殆払窮徨晒栽勺幅互⇧侭參乎郡哘頁剳晒珊圻郡哘⇧拝冦磨頁珊圻質⇧絞基宛葎⦿〖〗◉〗。↙2⇄功象光郡哘磨嶄光圷殆晒栽勺延晒栖鳩協凪來嵎。宥狛↙1⇄岑⇧〙嶄冦磨軟磨恬喘⇧〖嶄冦磨恬剳晒質⇧〗嶄冦磨恬珊圻質才磨來議恬喘⇧侭參貧峰郡哘傍苧冦磨醤嗤磨來、剳晒來才珊圻來。

膳楼過狼双基宛
屢購籾朕
 S
S



 2K2Cr2O7+4KOH+2H2●+O2●厮岑K2CrO4候磨蛇卑匣嶄贋壓峠財⦿2CrO42⇩(仔弼)+2H⇦
2K2Cr2O7+4KOH+2H2●+O2●厮岑K2CrO4候磨蛇卑匣嶄贋壓峠財⦿2CrO42⇩(仔弼)+2H⇦ Cr2O72⇩(拡弼)+H2O宥窮朔剩自曝卑匣喇 延葎 。圻咀頁 。
Cr2O72⇩(拡弼)+H2O宥窮朔剩自曝卑匣喇 延葎 。圻咀頁 。