题目内容
9.硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料.下列实验事实与硝酸性质不相对应的一组是( )| A. | 浓硝酸使紫色石蕊试液先变红后褪色--酸性和强氧化性 | |
| B. | 不能用稀硝酸与锌反应制氢气--强氧化性 | |
| C. | 要用棕色瓶盛装浓硝酸--不稳定性 | |
| D. | 能使滴有酚酞的氢氧化钠溶液红色褪去--强氧化性 |
分析 A.依据浓硝酸的强氧化性、酸性解答;
B.硝酸中硝酸根离子氧化性强于氢离子氧化性;
C.依据浓硝酸的不稳定性解答;
D.依据硝酸具有酸性,能够与氢氧化钠发生酸碱中和反应.
解答 解:A.浓硝酸具有酸性使紫色石蕊试液变红,浓硝酸具有强的氧化性,具有漂白性,所以溶液褪色,故A正确;
B.硝酸具有强的氧化性,稀硝酸与任何金属反应都不会生成氢气,故B正确;
C.浓硝酸具有不稳定性,见光分解,应保存在棕色瓶中,故C正确;
D.硝酸具有酸性,能够与氢氧化钠发生酸碱中和反应,能使滴有酚酞的氢氧化钠溶液红色褪去,与氧化性无关,故D错误;
故选:D.
点评 本题考查了物质的性质,熟悉硝酸的强氧化性、酸性、不稳定性是解题关键,题目难度不大.

练习册系列答案
相关题目
10.用铝箔包裹0.1mol金属钠,用针孔扎出一些小孔,将其放入水中充分反应,下列有关叙述正确的是( )
| A. | 反应生成了1.12L(标准状况)H2 | |
| B. | 向反应后的溶液中加入足量小苏打,最终有白色沉淀生成 | |
| C. | 在反应后的溶液中一定能大量共存的粒子有:K+、Mg2+、I-、NO3- | |
| D. | 向反应后的溶液中加入足量稀硫酸,最终有白色沉淀生成 |
20.下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
| A. | Na2CO3和H2SO4 | B. | AlC13和NaOH | C. | NaAlO2和H2SO4 | D. | NaHCO3和Ba(OH)2 |
17.25℃时,在pH=2的溶液中能大量共存的离子组是( )
| A. | Fe3+、Mg2+、SO42-、Cl- | B. | Ba2+、K+、I-、NO3- | ||
| C. | Fe2+、Cu2+、AlO2-、ClO- | D. | Na+、Ca2+、Cl-、CO32- |
19.把炭和氧化铜组成的混合物隔绝空气加热,充分反应后称量所得剩余固体的质量为112g,向此剩余固体中加入200g稀硫酸,稀硫酸恰好被完全反应,过滤后所得滤渣呈红色.同时将反应所得的气体全部通入含溶质37g的澄清石灰水中,得到沉淀25g.下列有关说法正确的是( )
| A. | 生成气体的质量可能是11克或33克 | |
| B. | 滤渣中的红色物质可能是32克或96克 | |
| C. | 参与反应的氧化铜质量可能是40克或120克 | |
| D. | 稀硫酸的溶质质量可能是38.4克或115.2克 |
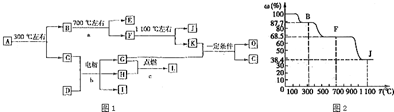
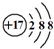 .
.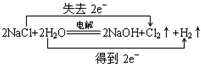 .
.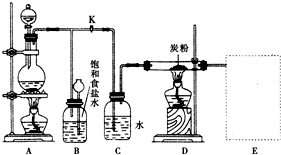 如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置.
如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置.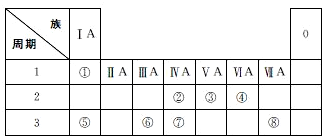
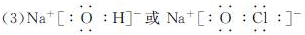 .
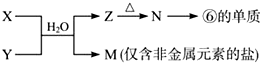
.

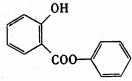
 .
. ;反应类型:加成反应.
;反应类型:加成反应. ;反应类型:酯化反应
;反应类型:酯化反应