题目内容
2.用惰性电极对0.06molAgNO3和0.02molKCl混合溶液300mL进行电解,电解一段时间后阴极析出3.24克金属,则此时溶液的PH值为多少?分析 电解混合溶液时,阴极发生Ag++e-=Ag,阳极发生:2Cl--2e-=Cl2↑、4OH--4e-=O2↑+2H2O,电解一段时间后阴极析出3.24克金属,即析出的是金属Ag,结合两极转移电子数目相等和电极方程式分析,并进行计算.
解答 解:0.06molAgNO3和0.02molKCl混合溶液中含有银离子的物质的量是0.06mol,含有氯离子的物质的量是0.02mol,阴极发生Ag++e-=Ag,阴极析出3.24g即0.03mol金属Ag,消耗银离子是0.03mol,转移电子是0.03mol,在阴极上银离子有剩余,在阳极上发生:2Cl--2e-=Cl2↑,氯离子的物质的量是0.02mol,全部失电子,转移电子是0.02mol,所以还会发生反应:4OH--4e-=O2↑+2H2O,转移电子0.01mol,消耗氢氧根离子是0.01mol,所以溶液中氢离子浓度是$\frac{0.01mol}{0.3L}$≈0.03mol/LpH=2-lg3=1.7,答:此时溶液的PH值为1.7.
点评 本题以电解原理为载体考查了物质的量的有关计算,明确离子放电顺序是解本题关键,结合转移电子守恒确定阳极上放电的离子,根据物质之间的关系式来分析解答,题目难度中等.

练习册系列答案
相关题目
12.对含氮物质的研究和利用有着极为重要的意义.
(1)N2、O2和H2相互之间可以发生化合反应,已知反应的热化学方程式如下:
N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1;
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1.
则氨的催化氧化反应的热化学方程式为4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905kJ/mol.
(2)汽车尾气净化的一个反应原理为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0.一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如图1所示.

①NO的平衡转化率为28.57%,0~20min平均反应速率v(NO)为0.02mol/(L•min).25min时,若保持反应温度不变,再向容器中充入CO、N2各0.8mol,则化学平衡将向左移动(填“向左”、“向右”或“不”).
②如图2若只改变某一反应条件X,反应由原平衡I达到新平衡Ⅱ,变量Y的变化趋势如表所示.下列说法正确的是b (填字母代号).
(3)某化学小组拟设计以N2和H2为电极反应物,以HCl-NH4Cl为电解质溶液制成燃料电池,则该电池的正极反应式为N2+8H++6e-═2NH4+.假设电解质溶液的体积不变,下列说法正确的是bcd(填字母代号).
a.放电过程中,电解质溶液的pH保持不变
b.溶液中的NH4Cl浓度增大,但Cl-离子浓度不变
c.每转移6.02×1023个电子,则有标准状况下11.2L电极反应物被氧化
d.为保持放电效果,电池使用一段时间需更换电解质溶液.
(1)N2、O2和H2相互之间可以发生化合反应,已知反应的热化学方程式如下:
N2(g)+O2(g)═2NO(g)△H=+180.5kJ•mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1;
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1.
则氨的催化氧化反应的热化学方程式为4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905kJ/mol.
(2)汽车尾气净化的一个反应原理为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0.一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如图1所示.

①NO的平衡转化率为28.57%,0~20min平均反应速率v(NO)为0.02mol/(L•min).25min时,若保持反应温度不变,再向容器中充入CO、N2各0.8mol,则化学平衡将向左移动(填“向左”、“向右”或“不”).
②如图2若只改变某一反应条件X,反应由原平衡I达到新平衡Ⅱ,变量Y的变化趋势如表所示.下列说法正确的是b (填字母代号).
| 条件X | 变量Y | |
| a | 压强 | 反应的平衡常数 |
| b | 温度 | CO的平衡浓度 |
| c | 温度 | N2的体积分数 |
| d | 催化剂 | NO的平衡转化率 |
a.放电过程中,电解质溶液的pH保持不变
b.溶液中的NH4Cl浓度增大,但Cl-离子浓度不变
c.每转移6.02×1023个电子,则有标准状况下11.2L电极反应物被氧化
d.为保持放电效果,电池使用一段时间需更换电解质溶液.
13.下列有关仪器的使用方法或实验操作正确的是( )
| A. | 用分液漏斗和烧杯分离水和乙酸乙酯的混合物 | |
| B. | 用瓷坩埚熔融烧碱 | |
| C. | 用玻璃棒蘸少量待测物质的浓溶液做焰色反应 | |
| D. | 将pH试纸直接插入溶液中测量某溶液pH |
10.下列关于水的电离叙述正确的是( )
| A. | 无论在什么条件下,c(H+)增大,酸性都增强 | |
| B. | 稀释氯化铵溶液,水的电离程度变大 | |
| C. | 稀释氢氧化钠溶液,水的电离程度变小 | |
| D. | 升高温度,KW变大,H+浓度增大 |
17.如表为元素A~G在周期表的位置,请回答有关问题:
(1)G元素原子结构示意图为 .
.
(2)B元素所形成氢化物的电子式为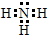 .
.
(3)C元素与F元素相比较,氢化物较稳定的是H2O>H2S(填氢化物的化学式).
(4)A、B、C三种元素的原子半径从小到大的顺序是C>N>O(用元素符号表示).
(5)D元素和E元素所形成的最高价氧化物的水化物碱性较强的是NaOH>Al(OH)3(用化学式表示).
(6)B元素的氢化物与G元素的氢化物反应所得生成物是离子(填“离子”或“共价”)化合物.
(7)D元素的过氧化物与水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | A | B | C | |||||
| 三 | D | E | F | G |
 .
.(2)B元素所形成氢化物的电子式为
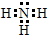 .
.(3)C元素与F元素相比较,氢化物较稳定的是H2O>H2S(填氢化物的化学式).
(4)A、B、C三种元素的原子半径从小到大的顺序是C>N>O(用元素符号表示).
(5)D元素和E元素所形成的最高价氧化物的水化物碱性较强的是NaOH>Al(OH)3(用化学式表示).
(6)B元素的氢化物与G元素的氢化物反应所得生成物是离子(填“离子”或“共价”)化合物.
(7)D元素的过氧化物与水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
2. 硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,该反应在沸腾炉中进行(填设备名称).
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂且有热交换器的接触室(填设备名称)中进行反应.在如图所示的装置中,C处流出的气体有SO3、SO2、O2;SO3进入吸收塔(填设备名称)用98.3%的H2SO4吸收,得到浓硫酸或发烟硫酸.
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是400℃,1个标准大气压.
(4)吸收塔排出的尾气中SO2的含量如果超过500μL/L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式2NH3•H2O+SO2=(NH4)2SO3+H2O.
 硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,该反应在沸腾炉中进行(填设备名称).
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂且有热交换器的接触室(填设备名称)中进行反应.在如图所示的装置中,C处流出的气体有SO3、SO2、O2;SO3进入吸收塔(填设备名称)用98.3%的H2SO4吸收,得到浓硫酸或发烟硫酸.
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是400℃,1个标准大气压.
| 压强/MPa SO2转化率 温度/℃ | 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9989 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8528 | 0.8897 | 0.9276 | 0.9468 |
9.工业上一般在恒容密闭容器中采用下列反应合成甲醇:
CO(g)+2H2(g)?CH3OH(g);△H
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)
某温度下,将2mol CO和6mol H2充人2L的密闭容器中,充分反应后,达到平衡时测得 c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提髙CO的转化率,可以采取的措施是df.
a.升温b.加人催化剂 c.增加CO的浓度 d.加入H2加压e.加人惰性气体加压 f.分离出甲醇
(4)300℃时,在一定的压强下,5mol CO与足量的H2在催化剂的作用下恰好完全反应变 化的热量为454KJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投人反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是D A.2c1>C3 B.a+b<90.8 C.2p2<p3 D.a1+a3<1.
CO(g)+2H2(g)?CH3OH(g);△H
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 35℃ |
| K | 2.041 | 0.270 | 0.012 |
(3)要提髙CO的转化率,可以采取的措施是df.
a.升温b.加人催化剂 c.增加CO的浓度 d.加入H2加压e.加人惰性气体加压 f.分离出甲醇
(4)300℃时,在一定的压强下,5mol CO与足量的H2在催化剂的作用下恰好完全反应变 化的热量为454KJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投人反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 2mol CH3OH | 2mol CH3OH | |
| 平 均 数 据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | aKJ | bKJ | cKJ | |
| 体系压强 | P1 | P2 | P3 | |
| 反转化率应物 | a1 | a2 | a3 | |