题目内容
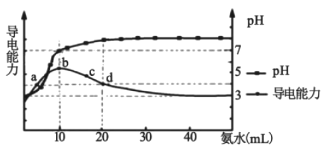
【题目】常温下,向10 mL0.1 mol/L的HR溶液中逐滴加入0.1 mol/L的氨水,所得溶液pH及导电能力变化如图。下列分析正确的是( )
A. 各点溶液中的阳离子浓度总和大小关系:d>c>b>a
B. 常温下,R- 的水解平衡常数数量级为10 -9
C. a点和d点溶液中,水的电离程度相等
D. d点的溶液中,微粒浓度关系:c(R-)+2c(HR)=c(NH3H2O)
【答案】B
【解析】
A.溶液导电能力与溶液中离子浓度有关,根据图象可知,b点导电能力最强,d点最弱,A错误;
B.根据图象可知,0.1mol/L的HR溶液的pH=3,则c(R-)≈c(H+)=10-3mol/L,c(HR)≈0.1mol/L,HR的电离平衡常数Ka=![]() =10-5,则R-的水解平衡常数数Kh=
=10-5,则R-的水解平衡常数数Kh=![]() =10-9,B正确;
=10-9,B正确;
C.a、d两点导电能力相等,但溶液的pH分别为4、8,都抑制了水的电离,a点c(H+)=10-4mol/L,d点c(OH-)=10-6mol/L,所以对水的电离程度的影响不同,C错误;
D.d点加入20mL等浓度的氨水,反应后溶质为等浓度的NH4R和NH3H2O,根据物料守恒可得:2c(HR)+2c(R-)=c(NH3H2O)+c(NH4+),因溶液呈碱性,NH3H2O的电离程度大于NH4+的水解程度,则c(NH4+)>c(NH3H2O),则c(HR)+c(R-)>c(NH3H2O),D错误;
故合理选项是B。

练习册系列答案
相关题目