题目内容
碳有多种单质,下列叙述正确的是(NA表示阿伏加德罗常数)
| A.72g C60中含有0.1NA个碳原子 |
| B.0.5 mol金刚石中含有2NA个碳碳单键 |
| C.1.2g由14C组成的单质中含有0.6 NA个中子 |
| D.在12g石墨片层结构中,含有六元环的个数为0.5 NA |
D
解析试题分析:A、72g C60中含有72÷12×NA="6" NA个碳原子,错误;B、0.5 mol金刚石中含有NA个碳碳单键(利用均摊法计算,一个碳原子形成4个碳碳单键,每个碳碳单键为两个碳原子共用,每个碳原子只占一半),错误;C、14C 的摩尔质量为14g/mol,错误;D、在石墨结构中每个碳原子3个环共用,故每个环包含碳原子数为6×1/3=2,在12g石墨片层结构中,含有六元环的个数为12÷12×NA÷2="0.5" NA,正确。
考点:考查阿伏加德罗常数有关问题。

练习册系列答案
相关题目
已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是( )
| A.16g | B.32g | C.64g /mol | D.32g /mol |
向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是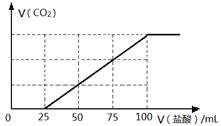
| A.原NaOH溶液的浓度为0.1 mol/L |
| B.通入CO2的体积为448 mL |
| C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3) =" 1:" 3 |
| D.所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) =" 2:" 1 |
设NA为阿伏加德罗常数的值。下列说法中正确的是( )
| A.在密闭容器中加入1 mol N2和3 mol H2,充分反应生成NH3分子数为2NA |
| B.标准状况下,22.4 L的CCl4分子中含有共价键数为4NA |
| C.常温常压下,1 mol NaHSO4晶体中含有2NA个离子 |
| D.电解饱和食盐水,当阴极产生2.24L H2时,转移的电子数一定为0.2NA |
常温常压下,往某密闭容器中充入两种气体,容器内最终气体的密度为2.2 g/L(折算到标准状况),则充入的气体一定不可能为
| A.NH3和HCl | B.NO和O2 | C.HI和Cl2 | D.SO2和H2S |
对于同温同压条件下的气体12C18O与14N2,判断正确的是
| A.体积相等时密度相等 | B.原子数相等时中子数相等 |
| C.体积相等时电子数相等 | D.质量相等时质子数相等 |
实验室里需用480 mL 0.1 mol/L的硫酸铜溶液,现选取500 mL容量瓶进行配制,以下操作正确的是( )
| A.称取7.68g硫酸铜,加入500mL水 |
| B.称取12.0g胆矾配成500mL溶液 |
| C.称取8.0g硫酸铜,加入500mL水 |
| D.称取12.5g胆矾配成500mL溶液 |
某风景区被称为天然氧吧,其原因是空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”。O2-就是一种空气负离子,其摩尔质量为
| A.32 g | B.32 g·mol-1 | C.33 g | D.33 g·mol-1 |
有两种金属组成的混合物粉末32g与足量的稀盐酸反应,生成11.2L(标况)H2,则该混合物的组成可能是:①Fe、Zn ②Al、Cu ③Ag、Mg ④Al、Fe
| A.①②③④ | B.①②③ | C.①③ | D.②③④ |