题目内容
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是( )
| A.气态氢化物稳定性:X > Y |
| B.元素非金属性:W >Y |
| C.原子半径的大小顺序为:r(Z)>r(W)>r(Q) |
| D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与NaOH溶液反应 |
AB
解析试题分析:根据所给的部分周期表图示,可以得出短周期元素X、Y、Z、W、Q分别为N、O、Al、S、Cl。根据元素周期律可得,非金属性Y>X,所以气态氢化物Y>X,A错误;非金属性Y>W,B错误;C、D均正确;故选AB。
考点:本题考查的是元素及其化合物的推断。

练习册系列答案
相关题目
推算原子序数为6、13、34、53、88的元素在周期表中的位置。
| 原子序数 | 6 | 13 | 34 | 53 | 88 |
| 周期 | | | | | |
| 族 | | | | | |
下列微粒的表示方法能确定为氧离子的是
| A.1S22S22p6 | B.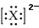 | C.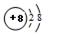 | D.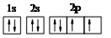 |
下列说法正确的是( )。
| A.Li是最活泼金属,F是最活泼非金属 |
| B.Mg(OH)2碱性比Ca(OH)2强 |
| C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 |
D.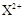 的核外电子数目为18,则X在第四周期第ⅡA族 的核外电子数目为18,则X在第四周期第ⅡA族 |
(双选)下列关于卤素的叙述正确的是( )。
| A.卤素只以化合态存在于自然界中 |
| B.随核电荷数增加,单质熔、沸点升高 |
| C.随核电荷数增加,单质氧化性增强 |
| D.单质与水反应,均可用通式X2+H2O=HX+HXO表示 |
气态原子生成+1价气态阳离子所需要的能量称为第一电离能。元素的第一电离能是衡量元素金属性强弱的一种尺度。下列有关说法正确的是 ( )
| A.元素的第一电离能越大,其金属性越强 |
| B.元素的第一电离能越小,其金属性越强 |
| C.金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关 |
| D.同周期元素,第一电离能随原子序数增大逐渐增大 |
19世纪中叶,门捷列夫的突出贡献是( )。
| A.提出原子学说 | B.提出分子学说 | C.发现元素周期律 | D.提出电离学说 |
在短周期元素中,若某元素原子的最外层原子数与其电子层数相等,则符合条件的元素种数为( )
| A.1种 | B.2种 | C.3种 | D.4种 |
X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z原子的最外层电子数是内层电子总数的三倍。下列有关叙述正确的是( )
| A.X、Y、Z三种元素可形成化合物X3YZ4 |
| B.X、Y两元素形成的化合物一定是离子化合物 |
| C.Y、Z两元素形成的化合物熔点较低 |
| D.稳定性:Y的氢化物>Z的氢化物 |