题目内容
16.回答下列问题:(1)用乙炔制备聚氯乙烯(
 )(自行选择无机原料),请书写化学反应方程式:
)(自行选择无机原料),请书写化学反应方程式: ,nCH2=CHCl$\stackrel{催化剂}{→}$
,nCH2=CHCl$\stackrel{催化剂}{→}$ ;
; (2实验室用乙醇制乙烯的反应方程式为
 .其反应类型为消去反应.检验生成的乙烯要将导管先后通入NaOH溶液、酸性KMnO4溶液或溴水.(填试剂名称)
.其反应类型为消去反应.检验生成的乙烯要将导管先后通入NaOH溶液、酸性KMnO4溶液或溴水.(填试剂名称)(3)由溴乙烷为原料合成1,2-二溴乙烷(自行选择无机原料),请书写化学反应方程式:
 ,
, ;
; (4)
 能发生反应生成一种含五元环的化合物,请书写化学反应方程式
能发生反应生成一种含五元环的化合物,请书写化学反应方程式 .
.
分析 (1)用乙炔和HCl先发生加成反应得CH2=CHCl,然后CH2=CHCl发生加聚反应即可;
(2)实验室用乙醇的消去反应制取乙烯,生成的乙烯中混有SO2,也能使溴水或高锰酸钾溶液褪色,故要先除去SO2;
(3)溴乙烷为原料合成1,2-二溴乙烷,先让溴乙烷发生消去反应制得乙烯,然后乙烯再与溴水加成即可;
(4) 能发生反应生成一种含五元环的化合物,是羧基和羟基发生了酯化反应,据此写出化学方程式.
能发生反应生成一种含五元环的化合物,是羧基和羟基发生了酯化反应,据此写出化学方程式.
解答 解:(1)用乙炔和HCl先发生加成反应得CH2=CHCl:
 ,故答案为:
,故答案为:
 ;
;
(2)实验室用乙醇的消去反应制取乙烯: ,反应类型为消去反应;由于生成的乙烯中混有SO2,而SO2也能使溴水或高锰酸钾溶液褪色,SO2的存在能干扰乙烯的检验,故要先用NaOH溶液除去SO2再用高锰酸钾溶液或溴水来检验乙烯的存在,故答案为:
,反应类型为消去反应;由于生成的乙烯中混有SO2,而SO2也能使溴水或高锰酸钾溶液褪色,SO2的存在能干扰乙烯的检验,故要先用NaOH溶液除去SO2再用高锰酸钾溶液或溴水来检验乙烯的存在,故答案为: ,消去反应,NaOH溶液,酸性KMnO4溶液或溴水.
,消去反应,NaOH溶液,酸性KMnO4溶液或溴水.
(3)溴乙烷为原料合成1,2-二溴乙烷,先让溴乙烷在NaOH乙醇溶液的作用下发生消去反应制得乙烯: ,然后乙烯再与溴水加成:
,然后乙烯再与溴水加成:
故答案为: ,
,
(4) 中羧基和羟基发生了酯化反应,化学方程式为:
中羧基和羟基发生了酯化反应,化学方程式为: ,故答案为:
,故答案为: .
.
点评 本题考查有机物的合成及结构与性质,为高频考点,把握有机物合成反应中官能团的变化、有机物官能团及性质为解答的关键,侧重常见有机物性质的考查,题目难度不大.

练习册系列答案
相关题目
6.现有烃的含氧衍生物A,还原A时得醇B,氧化A时得C,由B、C反应可生成高分子化合物,其结构简式为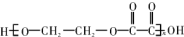 ,以下叙述错误的是( )
,以下叙述错误的是( )
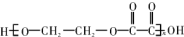 ,以下叙述错误的是( )
,以下叙述错误的是( )| A. | A属于醛类 | |
| B. | A有相对分子质量为58 | |
| C. | A分子中有6个原子含C 40% | |
| D. | 1molA与足量银氨溶液反应还原出4molAg |
7.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述不正确的是( )
| A. | 放电时负极反应为:Zn-2e-+2OH-═Zn(OH)2 | |
| B. | 放电时正极反应为:FeO${\;}_{4}^{2-}$+4H2O+3e-═Fe(OH)3+5OH- | |
| C. | 放电时正极附近溶液的碱性增强 | |
| D. | 放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
11.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g),△H1; 2H2(g)+O2(g)=2H2O(l),△H2 | |
| B. | S(g)+O2(g)=SO2(g),△H1; S(s)+O2(g)=SO2(g),△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g),△H1; C(s)+O2(g)=CO2(g),△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g),△H1; 2H2(g)+2Cl2(g)=4HCl(g),△H2 |
1.下列对于加成反应的说法中正确的是( )
| A. | 加成反应的结果是使有机化合物中不再含有不饱和键 | |
| B. | 福尔马林可以作为食品保鲜剂 | |
| C. | 甲苯在光照条件下与氯气反应,主要生成2,4-二氯甲苯 | |
| D. | 等物质的量的苯与苯甲酸完全燃烧消耗氧气的量相等 |
8.关于长式元素周期表的说法中不正确的是( )
| A. | 共有18个纵列,16个族 | |
| B. | 位于金属区和非金属区交界处的金属元素的族序数等于周期序数 | |
| C. | 过渡元素全是金属元素 | |
| D. | 第ⅢA族位于第3纵列 |
5.已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
| A. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{7}$amol | |
| B. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-})}$=$\frac{1}{2}$ | |
| C. | 参加反应的氯气的物质的量等于$\frac{1}{2}$amol | |
| D. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$amol≤ne≤amol |

 .
.