题目内容
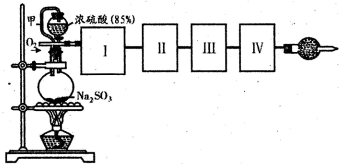
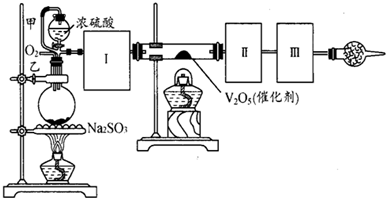
用如图装置可以进行测定SO2转化成SO3的转化率的实验.已知SO3的熔点是16.8℃,沸点是44.8℃.已知发生装置中所涉及反应的化学方程式为:Na2SO3(s)+H2SO4(85%)═Na2SO4+SO2↑+H2O
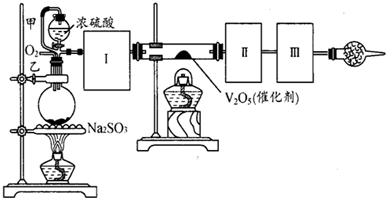
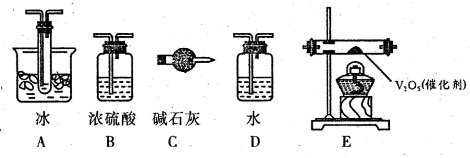
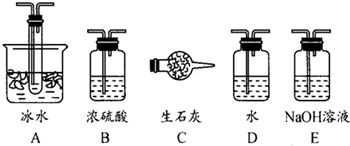
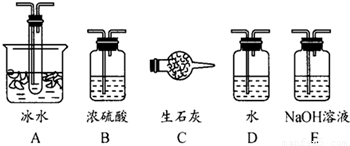
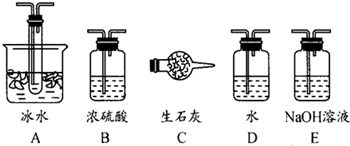
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从图A~E装置中选择最适合装置并将其序号填入下面的空格中.Ⅰ、Ⅱ、Ⅲ处连接的装置分别是
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(可以不填满).
①原因
②原因
③原因
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为
%(用含a、b的代数式填写)

(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从图A~E装置中选择最适合装置并将其序号填入下面的空格中.Ⅰ、Ⅱ、Ⅲ处连接的装置分别是
B
B
、A
A
、E
E
.
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是
先加热催化剂再滴入浓硫酸
先加热催化剂再滴入浓硫酸
.(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(可以不填满).
①原因
Na2SO3变质
Na2SO3变质
,验证方法取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液有白色沉淀生成,则证明该Na2SO3固体变质
取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液有白色沉淀生成,则证明该Na2SO3固体变质
;②原因
不是浓硫酸
不是浓硫酸
,验证方法用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸
用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸
;③原因
无
无
,验证方法无
无
.(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
SO2+2HClO3=H2SO4+2ClO2
SO2+2HClO3=H2SO4+2ClO2
.(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为
| 1600a-25b |
| 16a |
| 1600a-25b |
| 16a |
分析:(1)二氧化硫的干燥用浓硫酸,当温度低于16.8℃可以获得三氧化硫的晶体,尾气处理用烧碱溶液;
(2)为保证生成的二氧化硫尽可能的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作;
(3)亚硫酸钠变质会生成硫酸钠,根据检验亚硫酸钠中硫酸根是否存在来证明结论;亚硫酸钠和稀硫酸反应产生的二氧化硫速率很慢;
(4)SO2通入含1.0mol次氯酸的溶液中,根据转移的电子数来确定两种强酸;
(5)根据S元素守恒计算消耗的物质的量,可计算转化率.
(2)为保证生成的二氧化硫尽可能的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作;
(3)亚硫酸钠变质会生成硫酸钠,根据检验亚硫酸钠中硫酸根是否存在来证明结论;亚硫酸钠和稀硫酸反应产生的二氧化硫速率很慢;
(4)SO2通入含1.0mol次氯酸的溶液中,根据转移的电子数来确定两种强酸;
(5)根据S元素守恒计算消耗的物质的量,可计算转化率.
解答:解:(1)SO2转化成SO3之前必须对二氧化硫进行干燥,可以用浓硫酸,SO3的熔点是16.8℃,沸点是44.8℃,当温度低于 16.8℃时,三氧化硫以晶体状态存在,二氧化硫、三氧化硫的尾气处理用烧碱溶液吸收,故答案为:B;A;E;
(2)为保证生成的二氧化硫尽可能多的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作,保证生成的二氧化硫尽可能的参与反应,故答案为:先加热催化剂再滴入浓硫酸;
(3)影像化学反应速率的因素有:浓度、温度等,亚硫酸钠变质会生成硫酸钠,硫酸钠和浓硫酸不反应;此外亚硫酸钠和稀硫酸反应产生的二氧化硫速率会很慢,可能的原因是Na2SO3变质或不是浓硫酸;可通过取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质或者用洁净的玻璃棒沾取待测试样,滴到白纸上,如果不变黑,则证明该溶液不是浓硫酸,
故答案为:Na2SO3变质;取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质;不是浓硫酸;用洁净的玻璃棒沾取待测试样,滴到白纸上,如果不变黑,则证明该溶液不是浓硫酸;
(4)SO2通入含1.0mol次氯酸的溶液中,转移的电子为2mol,所以是1molSO2和1mol次氯酸反应生成盐酸和硫酸,
故答案为:SO2+H2O+HClO═HCl+H2SO4;
(5)根据元素守恒Na2SO3~SO2,则amol会生成二氧化硫amol,装置Ⅲ增重了bg,说明剩余的二氧化硫为bg
(即
=
mol),所以二氧化硫的转化率=
×100%=
%,
故答案为:
%(或者
×100%).
(2)为保证生成的二氧化硫尽可能多的转化为三氧化硫,应先加热催化剂再进行滴加浓硫酸操作,保证生成的二氧化硫尽可能的参与反应,故答案为:先加热催化剂再滴入浓硫酸;
(3)影像化学反应速率的因素有:浓度、温度等,亚硫酸钠变质会生成硫酸钠,硫酸钠和浓硫酸不反应;此外亚硫酸钠和稀硫酸反应产生的二氧化硫速率会很慢,可能的原因是Na2SO3变质或不是浓硫酸;可通过取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质或者用洁净的玻璃棒沾取待测试样,滴到白纸上,如果不变黑,则证明该溶液不是浓硫酸,
故答案为:Na2SO3变质;取待测试样于试管中,加适量的蒸馏水配成溶液,滴加足量的稀盐酸,再加入氯化钡溶液,如果有白色沉淀生成,则证明该亚硫酸钠已变质;不是浓硫酸;用洁净的玻璃棒沾取待测试样,滴到白纸上,如果不变黑,则证明该溶液不是浓硫酸;
(4)SO2通入含1.0mol次氯酸的溶液中,转移的电子为2mol,所以是1molSO2和1mol次氯酸反应生成盐酸和硫酸,
故答案为:SO2+H2O+HClO═HCl+H2SO4;
(5)根据元素守恒Na2SO3~SO2,则amol会生成二氧化硫amol,装置Ⅲ增重了bg,说明剩余的二氧化硫为bg
(即
| bg |
| 64g/mol |
| b |
| 64 |
a-
| ||
| a |
| 1600a-25b |
| 16a |
故答案为:
| 1600a-25b |
| 16a |
| 64a-b |
| 64a |
点评:本题主要考查了二氧化硫的性质以及离子的检验等知识,综合性较强,难度较大,考查学生分析和解决问题的能力.

练习册系列答案
相关题目
 不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10lkPa,温度为0℃,锌的相对原子质量为65).
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10lkPa,温度为0℃,锌的相对原子质量为65).