题目内容
按要求写出下列方程式:
(1)次氯酸的电离方程式 。
(2)氧化铝与氢氧化钠溶液反应的化学方程式 。
(3)二氧化锰与浓盐酸反应的离子方程式 。
(1)HClO H++ClO-( 2)Al2O3+2NaOH=2NaAIO2+H2O
H++ClO-( 2)Al2O3+2NaOH=2NaAIO2+H2O
(3)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
解析试题分析:(1)次氯酸是弱酸。电离时应该写可逆符号。电离方程式为HClO H++ClO-。(2)氧化铝是两性氧化物,既能与酸反应生成盐和水也能与碱反应生成盐和水。它与氢氧化钠溶液反应的化学方程式为Al2O3+2NaOH=2NaAIO2+H2O。(3)在实验室中氯气是用浓盐酸与二氧化锰共热制取的。反应的离子方程式为MnO2+4H++2Cl-
H++ClO-。(2)氧化铝是两性氧化物,既能与酸反应生成盐和水也能与碱反应生成盐和水。它与氢氧化钠溶液反应的化学方程式为Al2O3+2NaOH=2NaAIO2+H2O。(3)在实验室中氯气是用浓盐酸与二氧化锰共热制取的。反应的离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
考点:考查化学方程式和离子方程式的书写的知识。

练习册系列答案
相关题目
下列叙述中指定粒子数目一定大于NA的是
| A.11.2L氧气和臭氧的混合气体所含的原子数 |
| B.1mol CaC2固体中含阴离子总数 |
| C.1L1mol/LCH3COOH溶液中所含分子总数 |
| D.1molCl2参加化学反应获得的电子数 |
碘值是指100 g油脂中所能吸收(加成)碘的克数。测得某植物油碘值为a g,以NA表示阿伏加德罗常数,则b g该植物油中含有的碳碳双键数为
| A.abNA/25400 | B.abNA/12700 | C.abNA/2.54 | D.abNA/1.27 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.23gNO2和N2O4的混合气体中含有的氮原子数为0.5NA |
| B.4.2 g丙烯中所含的共用电子对总数为0.6NA |
| C.过氧化氢分解制得标准状况下1.12 L O2,转移电子数目为 0.2 NA |
| D.在高温、高压、催化剂的条件下,28gN2和6gH2充分反应,生成NH3的分子数为2NA |
设NA表示阿伏加德罗常数的数值,则下列说法中正确的是
| A.常温常压下,8.0g CH4中含有的氢原子数为2 NA |
| B.1 mol氯气跟水完全反应,转移的电子数为2 NA |
| C.1 mol Na2O2含离子数为4NA |
| D.0.1 mol/L MgCl2溶液中含氯离子数为0.2 NA |
下列有关化学用语表示正确的是
| A.葡萄糖的结构简式:C6H12O6 |
B.Cl-的结构示意图: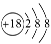 |
C.H2O2的电子式: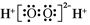 |
D.原子核中有10个中子的氧离子: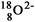 |
下列叙述中正确的是( )
| A.1 mol H2O的质量是18g/mol | B.硫酸根离子的摩尔质量是96g |
| C.CO2的摩尔质量是44g/mol | D.HCl的相对分子质量是36.5g/mol |
用NA表示阿伏加德罗常数的值。下列叙述中错误的是
| A.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA |
| B.在1 L 0.1 mol/L碳酸钠溶液中,阴离子总数大于0.1 NA |
| C.标准状况下,2.24 L Cl2分别与足量 Fe或Cu反应转移的电子数均为0.2NA |
| D.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体原子间的共用电子共6NA对 |