题目内容
【题目】下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
A | B | C | D | |
强电解质 | Fe | NaCl | CaCO3 | HNO3 |
弱电解质 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
非电解质 | C12H22O11(蔗糖) | BaSO4 | C2H5OH | H2O |
A.AB.BC.CD.D
【答案】C
【解析】
在水溶液中或熔融状态下导电的化合物为电解质;在水溶液中完全电离的电解质为强电解质。
A.Fe为单质,既不是电解质也不是非电解质,故A错误;
B.氨气为非电解质,硫酸钡为强电解质,故B错误;
C.碳酸钙为强电解质,磷酸为中强酸,属于弱电解质,酒精为非电解质,故C正确;
D.水是弱电解质,故D错误;
故答案为C。

 名校课堂系列答案
名校课堂系列答案【题目】某实验小组用工业上废渣(主要成分Cu2S和Fe2O3)制取纯铜和绿矾(FeSO4·7H2O)产品,设计流程如下:
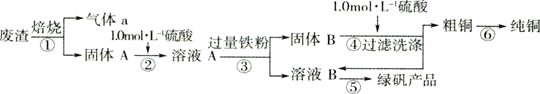
(1)在实验室中,欲用98%的浓硫酸(密度为1.84g·mL-1)配制500mL1.0mol·L-1的硫酸,需要取98%的浓硫酸______________mL(小数点后面保留一位有效数字);需要的仪器除量筒、烧杯、玻璃棒、胶头滴管,还有________。
(2)该小组同学设计如装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素。
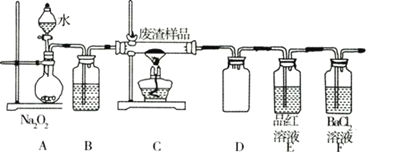
①置A中反应的化学方程式为_________;D装置起安全瓶作用____________ ,E装置中的现象是________
②反应装置不完善,为避免空气污染,要加装尾气处理装置所用试剂为________________溶液。
(3)从下列图中选择合适的装置,写出步骤⑤中进行的操作顺序 _______(填序号)
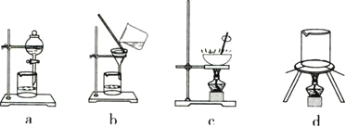
(4)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液体积/mL | 19.10 | 20.02 | 19.98 | 20.00 |
①第1组实验数据出现异常,造成这种异常的原因可能是________(填代号).
a.酸式滴管定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为________。
【题目】用下图表示的一些物质或概念间的从属关系中,不正确的是( )
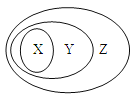
X | Y | Z | |
例 | 氧化物 | 化合物 | 纯净物 |
A | 苯的同系物 | 芳香烃 | 芳香族化合物 |
B | 烯烃 | 不饱和烃 | 烃 |
C | 减压蒸馏 | 常压蒸馏 | 石油的分馏 |
D | 油脂的皂化 | 酯的水解 | 取代反应 |
A. A B. B C. C D. D