题目内容
水热法制备Fe3O4纳米颗粒的总反应为:3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O32-+2H2O,下列说法正确的是
| A.x=2 | B.Fe2+、S2O32-都是还原剂 |
| C.硫元素被氧化,铁元素被还原 | D.每生成1 mol Fe3O4,则转移电子的物质的量为3 mol |
B
解析试题分析:A、根据电荷守恒可知,2×2+x-3×2=2,解得x=4,A不正确;B、反应中铁元素的化合价从+2价升高到+ 价,S2O32-中S元素的化合价从+2价升高到+
价,S2O32-中S元素的化合价从+2价升高到+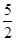 价,均被氧化,因此Fe2+、S2O32-都是还原剂,B正确;C、硫元素和铁都被氧化,氧气中氧元素被还原,C不正确;D、根据反应的方程式可知,每生成1 mol Fe3O4,参加反应的氧化剂氧气是1mol,则转移电子的物质的量为4 mol,D不正确,答案选B。
价,均被氧化,因此Fe2+、S2O32-都是还原剂,B正确;C、硫元素和铁都被氧化,氧气中氧元素被还原,C不正确;D、根据反应的方程式可知,每生成1 mol Fe3O4,参加反应的氧化剂氧气是1mol,则转移电子的物质的量为4 mol,D不正确,答案选B。
考点:考查氧化还原反应的有关判断和计算

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO 3Cu+N2+3H2O,对此反应的分析合理的是( )
3Cu+N2+3H2O,对此反应的分析合理的是( )
| A.该反应属置换反应 |
| B.CuO是氧化剂 |
| C.反应体现了金属铜的还原性 |
| D.每生成1molH2O就伴随着1mol电子转移 |
1 mo1Cu2S与2 mol FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2、
CuSO4的混合溶液,并产生NO气体。则最终反应所得NO物质的量为 ( )
| A.4 mo1 | B.5 mo1 | C.6 mo1 | D.7 mo1 |
某溶液中Cl-、Br-、I-三者物质的量之比是2∶3∶4,通入一定量的Cl2,该比值为1∶1∶1,则反应的Cl2和原溶液中I-的物质的量之比是 ( )
| A.1∶2 | B.1∶4 | C.1∶6 | D.1∶8 |
铋(Bi)最高化合价为+5价,其价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色.现取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应的现象如表所示:
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
则NaBiO3、KMnO4、I2、H2O2的氧化性由强到弱的顺序为( )
A.NaBiO3、KMnO4、H2O2、I2 B.KMnO4、NaBiO3、H2O2、I2
C.I2、H2O2、KMnO4、NaBiO3 D.KMnO4、NaBiO3、I2、H2O2
在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,1molCuSO4能氧化磷的物质的量是( )
A.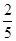 mol mol | B. mol mol | C.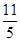 mol mol | D.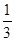 mol mol |
需要加入还原剂才能实现的变化是
| A.MnO2→MnO4— | B.AlO2—→Al(OH)3 | C.AsO43—→AsO33— | D.Cl—→Cl2 |
根据表中信息判断,下列选项不正确的是( )
| 序列 | 参加反应的物质 | 生成物 |
| ① | KMnO4 、H2O2 、H2SO4 | K2SO4 、MnSO4…… |
| ② | Cl2 、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- …… | Cl2 、Mn2+ …… |
A.第①组反应的其余产物为H2O和 O2
B.第②组反应中Cl2 与 FeBr2的物质的量之比为1︰2
C.第③组反应中生成1mol Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4- > Cl2 > Fe3+ > Br2
此反应:MnO2 +4 HCl(浓)  MnCl2 +Cl2↑+2H2 O,氧化剂和还原剂的物质的量比为
MnCl2 +Cl2↑+2H2 O,氧化剂和还原剂的物质的量比为
| A.4∶1 | B.1∶4 | C.1∶1 | D.1∶2 |