题目内容
7.用20g氢氧化钠固体配成1mol•L-1的NaOH溶液,所得溶液的体积是( )| A. | 1000 mL | B. | 500 mL | C. | 100 mL | D. | 50 mL |
分析 根据n=$\frac{m}{M}$计算出20g氢氧化钠的物质的量,再根据V=$\frac{n}{c}$计算出所配制的1mol•L-1的NaOH溶液的体积.
解答 解:20g氢氧化钠的物质的量为:$\frac{20g}{40g/mol}$=0.5mol,
用0.5mol氢氧化钠配制的成1mol•L-1的NaOH溶液的体积为:$\frac{0.5mol}{1mol/L}$=0.5L=500mL,
故选B.
点评 本题考查了物质的量浓度的简单计算,题目难度不大,试题侧重基础知识的考查,明确物质的量浓度的概念及表达式即可解答,注意熟练掌握物质的量与物质的量浓度、摩尔质量之间的转化关系.

练习册系列答案
相关题目
18.硫酸的消耗量是衡量一个国家化学工业发展水平的重要标志,H2SO4的相对分子质量为( )
| A. | 34 | B. | 98 | C. | 114 | D. | 128 |
15.我国酸雨形成的主要原因是( )
| A. | 汽车排出的大量尾气 | B. | 自然界中硫化物的分解 | ||
| C. | 工业上大量燃烧含硫的燃料 | D. | 制硝酸厂排出的大量尾气 |
2.将湿润的红色石蕊试纸放在进行下列实验的试管口,试纸变蓝色的有( )
| A. | 加热浓氨水 | B. | 加热NH4Cl固体 | ||
| C. | 加热NH4Cl和Ca(OH)2的混合物 | D. | 加热H2SO3溶液 |
12.下列金属元素中,不属于碱金属元素的是( )
| A. | Li | B. | Na | C. | Rb | D. | Mg |
16.医生建议患甲状腺肿大的病人多食海带,这是由于海带中含有较丰富的( )
| A. | 碘元素 | B. | 铁元素 | C. | 钾元素 | D. | 锌元素 |
2.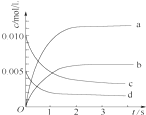 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)c({O}_{2})}$.已知:K(300℃)>K(350℃),则该反应正反应是放热反应.升高温度,正反应速率增大(填“增大”、“减小”或“不变”).
(2)如图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v(O2)=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是BC.
A.v(NO2)=2v(O2)
B.容器内压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂.
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v(O2)=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是BC.
A.v(NO2)=2v(O2)
B.容器内压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂.
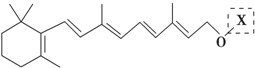 在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B(
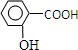
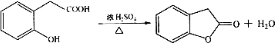
在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B(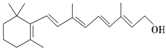 )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.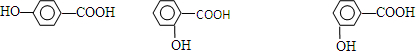 .
. .
. .
. .
.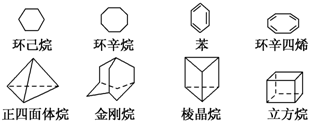 如图是八种环状的烃类物质:
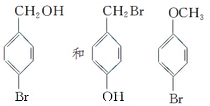
如图是八种环状的烃类物质: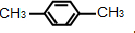 1,4-二甲苯、
1,4-二甲苯、 1,3,5-三甲苯.
1,3,5-三甲苯.