��Ŀ����
��10�֣����¶�һ���������£���һ�ܱ������м���4mol SO2 ��3 mol O2��������Ӧ��2 SO2 (g) + O2 (g) 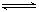 2
SO3 (g) ��H<O���ﵽƽ���������a
mol SO3��[��Դ:ѧ_��_��]
2
SO3 (g) ��H<O���ﵽƽ���������a
mol SO3��[��Դ:ѧ_��_��]
(1) �¶����ߣ��÷�Ӧ�Ļ�ѧƽ�ⳣKֵ___________(������С����������Ҳ���ܼ�С)��
��2��SO2��ת����Ϊ (����ĸa�ı���ʽ��ʾ)
��3�����÷�Ӧ���ں��º�ѹ���ܱ������н��еġ��ּ���8mol SO2��6mol O2 ���ﵽƽ���SO3��������ʵ���Ϊ mol (����ĸa��ʾ)������ͬ���������£�����3mol SO2��3mol O2��x molSO3���壬��ƽ���SO3�ڷ�Ӧ������е����������ԭƽ����ͬ����x= ��ƽ���SO3�����ʵ����� mol��(�ú�a�ı���ʽ��ʾ)
���𰸡�


��������

��ϰ��ϵ�д�
�����Ŀ
 ��֪����N2��g��+O2��g���T2NO��g����H1=+180kJ?mol-1
��֪����N2��g��+O2��g���T2NO��g����H1=+180kJ?mol-1��N2��g��+3H2��g��?2NH3��g����H2=-92.4kJ?mol-1
��2H2��g��+O2��g���T2H2O��g����H3=-483.6kJ?mol-1
����˵����ȷ���ǣ�������
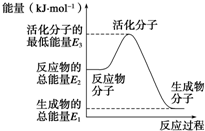
| A����Ӧ���е������仯��ͼ��ʾ�����H2=E1-E3 | B��H2��ȼ����Ϊ241.8 kJ?mol-1 | C���ɷ�Ӧ��֪���¶�һ���������£���һ�����ܱ�������ͨ��1 mol N2��3 mol H2����Ӧ��ų�������ΪQ1 kJ����ͨ��2 mol N2��6 mol H2��ַ�Ӧ��ų�������ΪQ2 kJ����184.8��Q2��2Q1 | D�����Ĵ�������ӦΪ4NH3��g��+5O2��g���T4NO��g��+6H2O��g����H=+906 kJ?mol-1 |
 2NH3(g)����H2����92.4 kJ��mol��1
2NH3(g)����H2����92.4 kJ��mol��1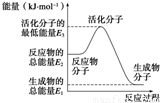
 cC��g���ﵽ��ѧƽ���C�����ʵ���Ũ��Ϊkmol��L��1�������¶�һ���������£����ܱ������ݻ���Ϊԭ����1/2��C�����ʵ���Ũ��Ϊ2kmol��L��1����ʼ�ղ��䡣��b��c��ϵ��
cC��g���ﵽ��ѧƽ���C�����ʵ���Ũ��Ϊkmol��L��1�������¶�һ���������£����ܱ������ݻ���Ϊԭ����1/2��C�����ʵ���Ũ��Ϊ2kmol��L��1����ʼ�ղ��䡣��b��c��ϵ��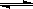 cC��g��
cC��g��