题目内容
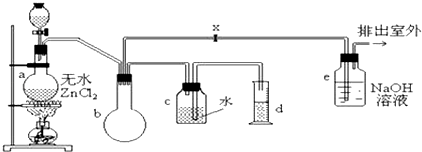
【题目】由碳、氢、氮三种元素组成的TMB是一种新型指纹检测的色原试剂,其相对分子质量为240.某研究性学习小组的同学欲利用下列装置测定TMB的分子式.实验原理:在足量氧气流中将4.80gTMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2 . 请从图中选择适当的装置(部分装置可以重复)进行实验. 
(1)仪器a的名称为 .
(2)实验装置依次连接的顺序为 .
(3)写出装置C中反应的化学方程式: .
(4)该实验(填“需要”或“不需要”)尾气处理,理由是 .
(5)实验后称得装置A的质量增加14.08g,装置B的质量增加3.60g并收集到0.56g氮气(假设每次吸收均是完全的),则TMB的分子式为 .
(6)设计实验验证CO2具有氧化性:
【答案】
(1)圆底烧瓶
(2)CBDBAA
(3)2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
(4)不需要;碳元素必须燃烧完全才能保证实验结果的准确性,没有有毒气体放出
(5)C16H20N2
(6)将打磨过的镁条点燃后深入充满二氧化碳的集气瓶中,镁条继续燃烧,集气瓶中有黑色固体生成为碳单质,说明二氧化碳具有氧化性
【解析】解:C中过氧化氢在二氧化锰催化作用下生成氧气,用浓硫酸干燥氧气,氧气将TMB氧化为二氧化碳、水和氮气,用碱石灰吸收二氧化碳,.根据A装置增加14.08g可以求出样品中C元素的物质的量,B装置增加3.60g可以求出样品中H元素的物质的量,再根据收集到0.56g氮气可以求出样品中N元素的物质的量,则TMB分子中碳、氢、氮的原子个数比就可以求出,根据相对分子质量之比算出相对分子质量,结合原子个数比计算出分子式,以此解答该题,(1)依据图形和作用可知,仪器a为圆底烧瓶,所以答案是:圆底烧瓶;(2)依据上述分析可知装置连接为制备氧气、干燥氧气、将TMB氧化、浓硫酸吸收生成的水蒸气、碱石灰吸收生成的二氧化碳气体、最后连接碱石灰防止空气中的二氧化碳和水蒸气进入装置A干扰测定结果,装置连接顺序为:CBDBAA,
所以答案是:CBDBAA;(3)过氧化氢在二氧化锰作用下分解生成水和氧气,反应的化学方程式为:2H2O2 ![]() 2H2O+O2↑,
2H2O+O2↑,
所以答案是:2H2O2 ![]() 2H2O+O2↑;(4)因二氧化碳完全吸收,且生成氮气是空气的成分,没有必要进行尾气处理,
2H2O+O2↑;(4)因二氧化碳完全吸收,且生成氮气是空气的成分,没有必要进行尾气处理,
所以答案是:不需要;因为碳元素必须燃烧完全才能保证实验结果的准确性,没有有毒气体排放;(5)实验后称得装置从用的先后顺序排列质量分别增加3.60g、14.08g,收集到0.56g氮气,则m(H2O)=3.60g,m(CO2)=14.08g,则
n(H2O)= ![]() =0.2mol,n(H)=0.4mol,
=0.2mol,n(H)=0.4mol,
n(CO2)= ![]() =0.32mol,n(C)=0.32mol,
=0.32mol,n(C)=0.32mol,
所以n(N)= ![]() =0.04mol,
=0.04mol,
则:n(C):n(H):n(N)=0.32mol:0.4mol:0.04mol=8:10:1,
TMB的相对分子质量为:2×120=240,设分子式为:C8nH10nNn , 则有:12×8n+10n+14n=240,解得n=2,所以分子式为C16H20N2 ,
所以答案是:C16H20N2;(6)设计实验使二氧化碳发生反应后碳元素化合价降低,做氧化剂,将打磨过的镁条点燃后深入充满二氧化碳的集气瓶中,镁条继续燃烧,集气瓶中有黑色固体生成为碳单质,说明二氧化碳具有氧化性,
所以答案是:将打磨过的镁条点燃后深入充满二氧化碳的集气瓶中,镁条继续燃烧,集气瓶中有黑色固体生成为碳单质,说明二氧化碳具有氧化性;

 阅读快车系列答案
阅读快车系列答案