题目内容
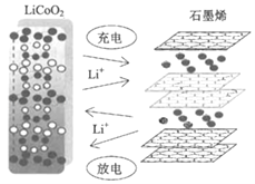
【题目】华为研发人员利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1﹣xCoO2C6+LiCoO2,其主要优势在于使用寿命长和充电速度快,其工作原理如图所示。下列关于该电池的说法错误的是( )
A.该电池若用隔膜,可选用阳离子交换膜
B.充电时,阴极反应为C6+xLi++xe﹣=LixC6
C.放电时,LiCoO2极发生的电极反应为:LiCoO2﹣xe﹣=Li1﹣xCoO2+xLi+
D.废旧的该电池进行“放电处理”,让Li+嵌入 LiCoO2中有利于回收石墨烯
【答案】C
【解析】
根据电池反应式及图示可知,负极反应为:LixC6 - xe﹣=C6+xLi+,正极反应为:Li1﹣xCoO2+xLi++ xe﹣=LiCoO2,充电时,阴阳极电极反应与负极正极反应式正好相反,据此分子判断。
A.根据图知,锂离子需要自由移动,所以需要阳离子交换膜,A项正确,不符合题意;
B.充电时,阴极上得电子发生还原反应,电极反应式为C6+xLi++xe﹣=LixC6,B项正确,不符合题意;
C.放电时,LiCoO2极得电子发生还原反应,发生的电极反应为:Li1﹣xCoO2+xLi++xe﹣=LiCoO2,C项错误,符合题意;
D.放电石墨烯为负极反应式为LixC6﹣xe﹣=C6+xLi+,所以放电处理让 Li+从石墨烯中脱出而有利于回收,D项正确,不符合题意;
答案选C。

【题目】反应CO(g)+2H2(g)![]() 2CH3OH(g)在恒容密闭容器中进行。为探究温度、CO2等因素对该反应的影响,进行了4组实验,结果如右下表。下列说法不正确的是
2CH3OH(g)在恒容密闭容器中进行。为探究温度、CO2等因素对该反应的影响,进行了4组实验,结果如右下表。下列说法不正确的是
组序号 | 1 | 2 | 3 | 4 | |
反应温度/℃ | 225 | 235 | 225 | 235 | |
反应前气体的物质的量/mol | CO2 | 0 | 0 | 0.2 | 0.2 |
CO | 3.0 | 3.0 | 2.8 | 2.8 | |
H2 | 7.0 | 7.0 | 7.0 | 7.0 | |
平衡时CH3OH的体积分数/% | 4.9 | 8.8 | 36.5 | 50.7 | |
A.该反应的△H>0
B.当容器中压强不变时,反应达到平衡
C.CH3OH含量增大的原因是CO2
D.少量CO2能提高平衡时CH3OH的体积分数
【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
I1 | I2 | I3 | I4 | I5 | |
电离能 | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是_________价,其基态原子电子排布式为_________。
(2)Ca3(PO4)3F中非金属元素电负性由大到小的顺序为_________。
(3)PO43-的中心原子的杂化方式为_________,该离子的空间构型为_________,键角为________,其等电子体有_________ (请写出两种)。
(4)CaF2晶胞结构如图所示,则CaF2晶体中与Ca2+最近且等距离的Ca2+数目为_________;已知Ca2+和F半径分别为a cm、b cm,阿伏加德罗常数为NA,M为摩尔质量,则晶体密度为________g·cm3(不必化简)。
(5)已知MgO与CaO的晶体结构相似,其摩氏硬度的大小关系为_________,原因为___________。