��Ŀ����
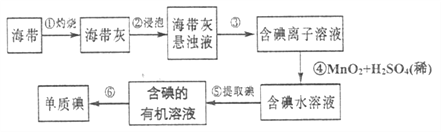
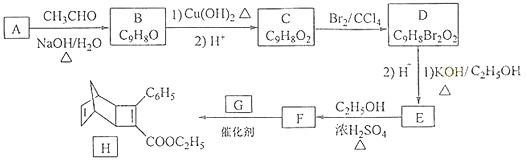
����Ŀ�����ú�ˮ������ȡ���þ����ȡ�������£�
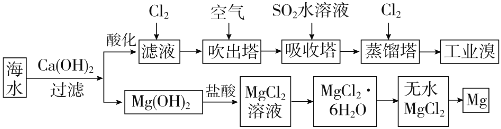
��1����ȡ��Ĺ����У�����2��![]() ת����Ŀ����__________���������з�����Ӧ�����ӷ���ʽ��
ת����Ŀ����__________���������з�����Ӧ�����ӷ���ʽ��![]() ���������з�����Ӧ�����ӷ���ʽ��____________��
���������з�����Ӧ�����ӷ���ʽ��____________��
��2����![]() ��Һ�еõ�
��Һ�еõ�![]() �������Ҫ������__________��_________�����ˡ�ϴ�ӡ��������ˮ�Ȼ�þ�õ�þ�Ļ�ѧ����ʽ��__________��
�������Ҫ������__________��_________�����ˡ�ϴ�ӡ��������ˮ�Ȼ�þ�õ�þ�Ļ�ѧ����ʽ��__________��
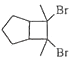
��3�����������̣���![]() ��ˮ����Ԫ�أ���ˮ��
��ˮ����Ԫ�أ���ˮ��![]() ���Ӻ���Ϊ
���Ӻ���Ϊ![]() ��ת��Ϊ��ҵ�壬����������������Ҫ��״����
��ת��Ϊ��ҵ�壬����������������Ҫ��״����![]() �����Ϊ_________L������
�����Ϊ_________L������![]() �ܽ⣩��
�ܽ⣩��
���𰸡� ����Ԫ�ؽ��и��� ![]() ����Ũ�� ��ȴ�ᾧ
����Ũ�� ��ȴ�ᾧ ![]() 179.2
179.2
����������ˮ�м����������Ƴ���þ���Ӻ���ˣ�����Һ��ͨ�������ǽ���Һ�е�Br-����ΪBr2���������ȵĿ�����Br2������������������SO2��Ӧ���䷴Ӧ�����ӷ���ʽΪ��SO2+Br2+2H2O=2HBr+H2SO����ͨ��������Br-����ΪBr2������Br-��Br2ת����Ŀ���Ƕ���Ԫ�ؽ��и�����������þ���������ܽ�õ��Ȼ�þ��Һ���Ȼ�þ��Һ�еõ��Ȼ�þ����IJ����Ǽ���������ȴ�ᾧ�õ���ˮ�Ȼ�þ����������Ȼ�þ�õ�����þ��
��1���������Ϸ�����֪��������ȡ��Ĺ����У�����2��Br-��Br2ת����Ŀ����Ϊ�˵õ�������嵥�ʣ���ȡ���̶���Ԫ�ؽ��и�������������ͨ��Ķ������������Ǻ��嵥�ʷ�Ӧ���������ӣ����������б����������õ�������嵥�ʣ���Ӧ�����ӷ���ʽ��Cl2+2Br����Br2+2Cl������2����MgCl2��Һ�еõ�MgCl26H2O�������Ҫ����������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵõ�����������Ȼ�þ�õ�����þ����������Ӧ�Ļ�ѧ����ʽΪ��MgCl2�����ڣ�![]() Mg+Cl2������4������10m3��ˮ�е���Ԫ��ת��Ϊ��ҵ�壬������Ԫ�غ���Ϊ64mg/L��10m3��ˮ�к���Ԫ��=10��1000L��64g/L��10-3=640g�����ʵ���=640g��80g/mol=8mol�����ݷ�Ӧ����õ���Cl2+2Br����Br2+2Cl���������������ʵ���Ϊ��4mol����ȡ��������Ҫ����ͨ������ʵ�������ӱ�����������������Ҫ��״����Cl2�����ʵ���Ϊ8 mol����״�������Ϊ8mol��22.4L/mol=179.2L��
Mg+Cl2������4������10m3��ˮ�е���Ԫ��ת��Ϊ��ҵ�壬������Ԫ�غ���Ϊ64mg/L��10m3��ˮ�к���Ԫ��=10��1000L��64g/L��10-3=640g�����ʵ���=640g��80g/mol=8mol�����ݷ�Ӧ����õ���Cl2+2Br����Br2+2Cl���������������ʵ���Ϊ��4mol����ȡ��������Ҫ����ͨ������ʵ�������ӱ�����������������Ҫ��״����Cl2�����ʵ���Ϊ8 mol����״�������Ϊ8mol��22.4L/mol=179.2L��