题目内容
【题目】l00mL稀H2S04和稀HC1的混合溶液中,部分离子的浓度关系如图所示, 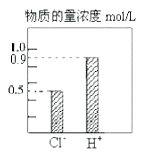
(1)原混合液中H2SO4的物质的量浓度为多少 mol/L:
(2)向其中加入8.55g Ba(OH)2粉末,充分反应后,所得溶液中OH﹣的物质的量.(假设反应前后溶液体积不变,要求写出计算过程).
【答案】
(1)解:根据图示可知,混合液中氯离子的物质的量为0.5mol,根据质量守恒可知混合液中含有HCl的物质的量为0.5mol,既混合液中HCl电离出的氢离子为0.5mol,则硫酸电离出的氢离子的物质的量为:0.9mol﹣0.5mol=0.4mol,混合液中含有硫酸的物质的量为:n(H2SO4)=0.4mol× ![]() =0.2mol,原混合液中H2SO4的物质的量浓度为:c(H2SO4)=
=0.2mol,原混合液中H2SO4的物质的量浓度为:c(H2SO4)= ![]() =0.2mol/L,
=0.2mol/L,
答:原混合液中H2SO4的物质的量浓度为0.2mol/L
(2)解:8.55g Ba(OH)2的物质的量:n(Ba(OH)2)= ![]() =0.05mol,含有氢氧根离子的物质的量为:0.05mol×2=0.1mol,反应后溶液中氢氧根离子的物质的量为:0.1mol﹣0.9mol=0.1mol,
=0.05mol,含有氢氧根离子的物质的量为:0.05mol×2=0.1mol,反应后溶液中氢氧根离子的物质的量为:0.1mol﹣0.9mol=0.1mol,
答:充分反应后,所得溶液中OH﹣的物质的量为0.01mol
【解析】(1)根据氯离子守恒判断HCl的物质的量,然后根据氢离子的物质的量计算出硫酸的物质的量,最后根据c= ![]() 计算出原混合液中H2SO4的物质的量浓度;(2)先根据n=
计算出原混合液中H2SO4的物质的量浓度;(2)先根据n= ![]() 计算出8.55g Ba(OH)2的物质的量,然后可知氢氧根离子的物质的量,再根据中和反应实质计算出充分反应后所得溶液中氢氧根离子的物质的量.
计算出8.55g Ba(OH)2的物质的量,然后可知氢氧根离子的物质的量,再根据中和反应实质计算出充分反应后所得溶液中氢氧根离子的物质的量.

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(gmol﹣1) |
蔗糖(C12H22O11) | 25.00 | 342 |
硫酸钾 | 0.84 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.075 | 170 |
(1)配制1L上述“鲜花保鲜剂”所需的仪器有:量筒、玻璃棒、药匙、烧杯、托盘天平、、 . (在横线上填写所缺仪器的名称).
(2)在溶液配制过程中,卜^列操作对配制结果没有影响的是 .
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(3)一鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为mol/L.
