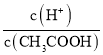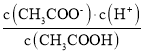题目内容
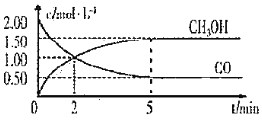
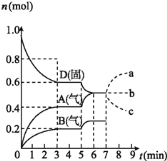
【题目】在1.0 L恒容密闭容器中投入1 mol CO2和 2.75 mol H2发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量如图所示。下列说法正确的是
CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量如图所示。下列说法正确的是
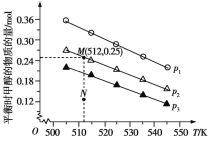
A. 该反应的正反应为吸热反应 B. 压强大小关系为p1<p2<p3
C. M点对应平衡常数K的值约为1.04×10-2 D. 在p2及512 K时,图中N点v正<v逆
【答案】C
【解析】
A、压强不变时,升高温度,平衡时甲醇的物质的量减小,平衡逆向移动,说明该反应的正反应为放热反应,故A错误;B、温度不变时,增大压强,平衡正向移动,平衡时甲醇的物质的量增大,则p3<p2<p1,故B错误;C、M点时,n(CH3OH)=0.25 mol,据此计算出各物质的平衡浓度分别为c(CO2)=0.75 mol/L,c(H2)=2 mol/L,c(CH3OH)=c(H2O)=0.25 mol/L,K=![]() ≈1.04×10-2,故C正确;D、在p2及512 K时,图中N点甲醇的物质的量比平衡时的物质的量小,反应正向移动才能达到平衡,此时v逆<v正,故D错误。
≈1.04×10-2,故C正确;D、在p2及512 K时,图中N点甲醇的物质的量比平衡时的物质的量小,反应正向移动才能达到平衡,此时v逆<v正,故D错误。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
某化学小组根据上述反应原理进行下列实验:
I.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol/LKMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在______(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会______(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为_______________________________。
(4)计算H2C2O4溶液的物质的量浓度为__________mol/L。
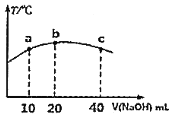
II.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号 | 体积V/mL | |||
0.1molL-1KMnO4溶液 | 0.11molL-1H2C2O4溶液 | 0.11molL-1H2SO4溶液 | H2O | |
① | 2.0 | 5.0 | 6.0 | 7.0 |
② | 2.0 | 8.0 | 6.0 | V1 |
③ | 2.0 | V2 | 6.0 | 2.0 |
请回答:
(5)表中v1=______。
(6)实验中需要测量的数据是______________________________。
(7)实验中______(填“能”或“不能”)用0.2mol/L盐酸代替0.1mol/LH2SO4溶液,理由是_________。
【题目】二氧化碳的回收利用是环保领域研究的热点课题。
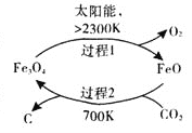
(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如右图所示,其总反应的化学方程式为_________。
(2)CO2经过催化氢化合成低碳烯烃.其合成乙烯的反应为2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g)△H,已知几种化学键键能如下表所示:(CO2的结构式:O=C=O)
CH2=CH2(g)+4H2O(g)△H,已知几种化学键键能如下表所示:(CO2的结构式:O=C=O)
物质 | H-H | C=O | C=C | C-H | H-O |
能量/kJmol-1 | 436 | 745 | 615 | 413 | 463 |
则△H=_________。
(3)在2L恒容密闭容器中充入2molCO2和n molH2,在一定条件下发生(2)中的反应,CO2的转化率与温度、投料比[X= ![]() ]的关系如图所示。
]的关系如图所示。

①X1_________X2(填“>”、“<”或“=”,下同),平衡常数KA_________KB.
②若B点的投料比为3,且从反应开始到B点需要10min,则v(H2)=_______ molL-1·min-1。
(4)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如下图。(丙烯的结构简式:CH3CH=CH2)
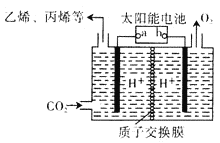
①b电极的名称是_________;
②产生丙烯的电极反应式为_______________。