题目内容
某化学反应2A (g) ≒ B(g) + D(g) 在4种不同条件下进行,B和D的起始浓度为0 ,反应物A 的浓度(mol?L-1) 随反应时间 (min) 的变化情况如下表:
根据上述数据,完成下列填空:
(1)实验1达到平衡的时间是 min,实验4达到平衡的时间是 min,
C3 1.0 mol?L-1(填“ < ”、“ > ”或“ = ” )。
(2)实验4比实验1的反应速率 (填“快”或“慢”),原因是 。
| 实验 序号 | 浓度
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 | ||
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 | ||
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 | ||
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)实验1达到平衡的时间是 min,实验4达到平衡的时间是 min,
C3 1.0 mol?L-1(填“ < ”、“ > ”或“ = ” )。
(2)实验4比实验1的反应速率 (填“快”或“慢”),原因是 。
(1) 40 min, 30 min,C3 大于 1.0 mol?L-1
(2) 快 (填“快”或“慢”),
原因是 反应温度 高 且先达到平衡 。
试题分析:(1)达平衡指的是物质量浓度不再变化,所以为40min后,实验4达平衡的时间为30min,也是浓度不再变化的时候。比较实验3和实验2,在10min到20min时,实验三反应速率快,所以一开始浓度比实验2的浓度大。
(2)温度越高,影响反应速率,反应速率越快。达平衡的时间越短。
点评:本题属于简单的化学反应平衡的试题,主要要会将表格看懂,比较不同实验,找到实验的固定量和变化量。最后抓住化学反应平衡状态的特征来解题。

练习册系列答案
相关题目
 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( ) 2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )
2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )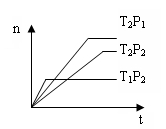
 2S(g)+R(s)下列说法可以说明反应已达平衡的是
2S(g)+R(s)下列说法可以说明反应已达平衡的是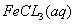 与
与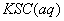 混合时存在下列平衡:
混合时存在下列平衡: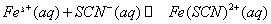 。已知平衡时,物质盼量浓度
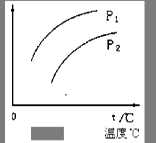
。已知平衡时,物质盼量浓度 与温度T的关系如右图所示,则下列说法正确的是
与温度T的关系如右图所示,则下列说法正确的是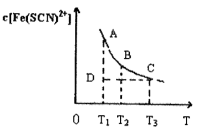

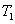 、
、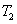 时,反应的平衡常数分别为
时,反应的平衡常数分别为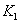 、
、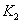 ,则
,则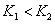
 大
大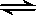 2C(g),达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法正确的是
2C(g),达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则下列说法正确的是  mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据: CO2(g)+H2(g)下列情况中,能说明反应达到化学平衡状态的是
CO2(g)+H2(g)下列情况中,能说明反应达到化学平衡状态的是 2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是:( )
2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是:( )