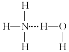题目内容
【题目】工业上用铝土矿(主要成分是氧化铝,含氧化铁杂质)为原料冶炼铝的工艺流程如下:
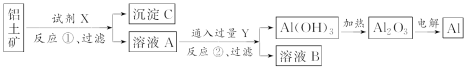
下列叙述正确的是( )
A. 反应①中试剂X是氢氧化钠溶液
B. 试剂Y是HCl,它与AlO![]() 反应生成氢氧化铝
反应生成氢氧化铝
C. 图中所示转化反应中包含2个氧化还原反应
D. 将X与Y试剂进行对换,最终可以达到相同结果
【答案】A
【解析】
试题 A.试剂X不能是盐酸,因氧化铝、氧化铁都能与盐酸反应,溶液中溶质为氯化铝、氯化铁和盐酸,反应②无法实现生成氢氧化铝和碳酸氢钠,正确;B. 试剂Y是HCI,它与AlO2-反应生成Al3+,C. 图中所示转化有一步是氧化还原反应:2Al2O3![]() 4Al+3O2↑,错误;D.试剂X为氢氧化钠,沉淀为氧化铁,溶液为偏铝酸钠和氢氧化钠混合溶液,通入过量二氧化碳气体,NaOH+CO2=NaHCO3、NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,不能调换错误;选A
4Al+3O2↑,错误;D.试剂X为氢氧化钠,沉淀为氧化铁,溶液为偏铝酸钠和氢氧化钠混合溶液,通入过量二氧化碳气体,NaOH+CO2=NaHCO3、NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,不能调换错误;选A

练习册系列答案
相关题目