题目内容
【题目】下列关于Na2CO3 和NaHCO3的叙述不正确的是
A.在相同情况下,Na2CO3 比NaHCO3易溶于水
B.温度相同,浓度相同Na2CO3 溶液的碱性比NaHCO3溶液碱性强
C.可用相同的离子方程式表示Na2CO3 和NaHCO3分别与Ca(OH)2溶液的反应
D.等质量的Na2CO3 和NaHCO3分别与足量的盐酸溶液反应,后者放出的CO2多
【答案】C
【解析】
A.常温下,Na2CO3较NaHCO3易溶于水,故A正确;
B.Na2CO3和NaHCO3都为强碱弱酸盐,水解呈碱性,且Na2CO3水解程度比NaHCO3大,则温度相同,浓度相同Na2CO3溶液的碱性比NaHCO3溶液碱性强,故B正确;
C.Na2CO3和NaHCO3与氢氧化钙溶液反应的离子方程式分别为:![]() 、
、![]() ,故C错误;
,故C错误;
D.根据反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑,等物质的量的Na2CO3和NaHCO3分别与过量盐酸反应,生成的二氧化碳一样多,则等质量的Na2CO3和NaHCO3分别与过量盐酸反应,后者放出的CO2多,故D正确;
答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
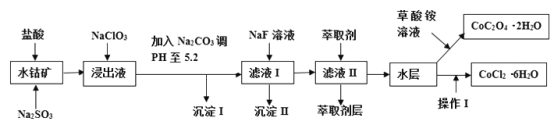
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;②沉淀I中只含有两种沉淀;③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中Co2O3发生反应的离子反应方程式为_________________。
(2)NaClO3在浸出液中发生的离子反应方程式为______________。
(3)加入Na2CO3调PH至5.2,目的是________;萃取剂层含锰元素,则沉淀II的主要成分为_____。
(4)操作I包括:将水层加入浓盐酸调整PH为2-3,______、_____、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是_____(回答一条原因即可)。