题目内容
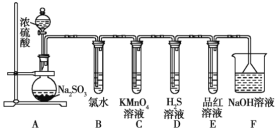
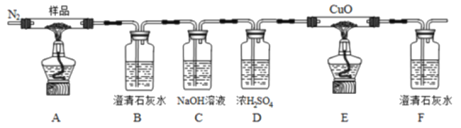
【题目】为了探究Cl2、SO2同时通入水中所发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
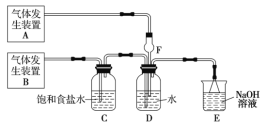
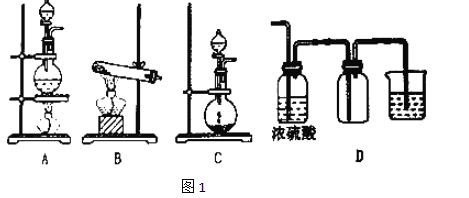
(1)该化学兴趣小组的同学采用Na2SO3与质量分数为70%的硫酸为原料制取SO2,采用MnO2与浓盐酸为原料制取Cl2。在此实验中,仪器![]() 的作用是______;气体发生装置B应选择下列装置中的____________(填序号)。
的作用是______;气体发生装置B应选择下列装置中的____________(填序号)。
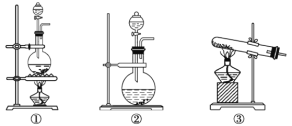
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,该化学兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有______(填序号)的试管中,再加入______(填序号),产生的现象是______。
若SO2过量,取适量D中溶液滴加至盛有______(填序号)的试管中,产生的现象是______。
【答案】防止倒吸 ① ② ③ 溶液呈红色 ①(或④) 溶液由棕黄色变成浅绿色(或溶液的紫色褪去)
【解析】
二氧化硫易溶于水,在装置D中有防倒吸装置F,则装置A为制取二氧化硫装置,装置A为制取氯气的装置;装置C为吸收HCl气体杂质的装置,E为尾气吸收装置。
(1)气体发生装置B中产生的气体用饱和食盐水进行除杂净化,可知B装置为制取Cl2的装置,则A装置为制取SO2的装置,因SO2易溶于水,故仪器F的作用是防止倒吸。制取Cl2所用的试剂为MnO2和浓盐酸,是固、液混合加热制取气体,故应选①装置为发生装置。
(2)若Cl2过量,则装置D的溶液中除含有H2SO4、HCl外,还含有剩余的Cl2,Cl2具有强氧化性,可将Fe2+氧化为Fe3+,故可选择②③进行检验;若SO2过量,则D装置的溶液中含有SO2、H2SO3,SO2具有还原性,故可选用①或④进行检验。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目