题目内容
4.五种如表所示的短周期主族元素,下列说法不正确的是( )| X | L | Z |
| Y | W |
| A. | Y的原子半径一定比L的大 | |
| B. | 若 X、Y为非金属元素,则X、Y元素形成的单质晶体类型一定相同 | |
| C. | 若X、W能组成XW2型分子,则其空间构型一定为直线型 | |
| D. | 对应简单氢化物的沸点可能是 X>Y、Z>W |
分析 A.电子层越多,原子半径越大;
B.若 X、Y为非金属元素,为同主族元素,可能为C、Si;
C.若X、W能组成XW2型分子,应为CS2;
D.X可能为C,甲烷中不含氢键,而Z的氢化物含氢键.
解答 解:A.电子层越多,原子半径越大,则Y的原子半径一定比L的大,故A正确;
B.若 X、Y为非金属元素,为同主族元素,可能为C、Si,若单质分别为C60、Si,X、Y元素形成的单质晶体类型分别为分子晶体、原子晶体,故B错误;
C.若X、W能组成XW2型分子,应为CS2,由二氧化碳为直线结构可知,其空间构型一定为直线型,故C正确;
D.X可能为C,甲烷中不含氢键,若X为N,则Z为F,N、F的氢化物含氢键,则沸点可能是 X>Y、Z>W,故D正确;
故选B.
点评 本题考查元素周期表的结构、位置与性质,为高频考点,把握元素的位置、元素周期律、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意D中含氢键的物质沸点高,题目难度不大.

练习册系列答案
相关题目
15.为了实现绿色化学,符合工业生产实际的是( )
| A. | 用纯碱吸收硫酸工业的尾气 | B. | 用烧碱吸收氯碱工业的尾气 | ||
| C. | 用纯碱吸收合成氨工业的尾气 | D. | 用烧碱吸收炼铁工业的尾气 |
19.如图表示M的结构简式,下列有关M的说法正确的是( )
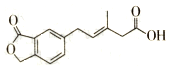

| A. | M可以发生加成、加聚、水解、酯化等反应 | |
| B. | l mol M最多可以与3 mol NaOH反应 | |
| C. | M苯环上的一氯取代物有两种不同结构 | |
| D. | l molM最多可以与5 mol H2发生加成反应 |
9.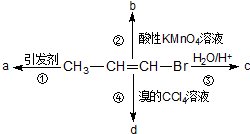 1-溴丙烯能发生如下图所示的4个不同反应.已知产物a为高分子化合物,则产物中只含有一种官能团的反应是( )
1-溴丙烯能发生如下图所示的4个不同反应.已知产物a为高分子化合物,则产物中只含有一种官能团的反应是( )
 1-溴丙烯能发生如下图所示的4个不同反应.已知产物a为高分子化合物,则产物中只含有一种官能团的反应是( )
1-溴丙烯能发生如下图所示的4个不同反应.已知产物a为高分子化合物,则产物中只含有一种官能团的反应是( )| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
16.某化学式为C3H6O2的有机物的PMR谱有三个信号蜂,其强度比为3:2:1,则该有机物的结构简式不可能是( )
| A. | CH3CH2COOH | B. | CH3COOCH3 | C. | HCOOCH2CH3 | D. | CH3COCH2OH |
13. 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )| A. | 该混合气体中一定含有乙烯 | |
| B. | 该混合气体中有且只有一种烷烃 | |
| C. | 组成该混合气体的烃分子所含氢原子数均为4 | |
| D. | 若混合气体由CH4和C2H4组成,则其体积比为2:3 |
14.对于H3O+的下列说法中正确的是( )
| A. | O原子采用SP2杂化 | B. | O原子采用SP3杂化 | ||
| C. | 离子中不存在配位键 | D. | 离子中存在非极性键 |
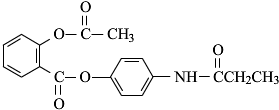 ,由它可衍生出一系列物质,有关变化如图:
,由它可衍生出一系列物质,有关变化如图: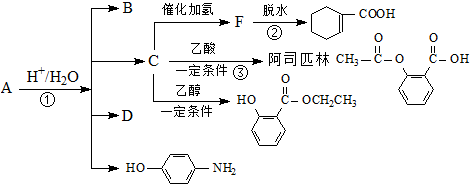
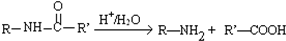
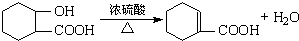 .
.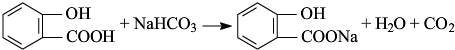 .
.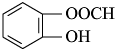 (或间位或对位).
(或间位或对位).